Согласно исследованию, новый антибиотик избавляет мышей от гонореи с множественной лекарственной устойчивостью после одной пероральной дозы.
Центр по контролю и профилактике заболеваний США (CDC) включил гонорею с множественной лекарственной устойчивостью в число пяти наиболее опасных на сегодняшний день угроз. Новое соединение нацелено на молекулярный механизм, обнаруженный у бактерий, но не у человека, и может привести к новому методу лечения гонореи и инфекций, вызванных другими бактериями, такими как туберкулез и MRSA. Исследовательская группа, в состав которой также вошли специалисты из биофармацевтической компании Microbiotix, опубликовала свои результаты в статье в журнале Nature Communications.
"Многие современные антибиотики нацелены на процесс трансляции - создания белков на основе информации в генетическом материале бактерий", - говорит Кен Кейлер, автор статьи. "В последнее десятилетие мы изучаем семейство соединений, которые вместо этого ингибируют транс-трансляционный механизм у бактерий, которые они используют для исправления определенных видов ошибок при синтезе белков. В данной работе мы приводим доказательство концепции, что ингибирование транс-трансляции может эффективно устранить гонорею с множественной лекарственной резистентностью у животных".
Ранее исследователи выявили многообещающий ингибитор транс-трансляции, который устраняет возбудитель гонореи в лабораторных культурах, но неэффективен у животных, поскольку соединение распадается. В данном исследовании члены исследовательской группы компании Microbiotix внесли стратегические изменения в соединение, чтобы определить, какие части его структуры необходимы для ингибирования механизма, а какие могут быть изменены для улучшения его стабильности.
"Наша работа по оптимизации изучила более 500 версий препарата, чтобы оценить их потенциал, токсичность и другие фармакологические свойства", - говорит Закари Арон, соавтор статьи. Мы определили, что центральная область соединения играет решающую роль в блокировании пути трансляции, однако модификации на периферии могут быть изменены для модуляции его фармакологических свойств. Изменяя функциональную группу, мы можем создать гораздо более устойчивые у животных варианты соединения".
Затем члены исследовательской группы протестировали на мышах одно из этих модифицированных соединений, MBX-4132. В своих экспериментах они использовали штамм гонореи WHO-X, чрезвычайно вирулентный патоген, устойчивый почти ко всем одобренным антибиотикам. Однократная пероральная доза препарата полностью устранила инфекцию у 80% мышей в течение шести дней, а бактериальная нагрузка у оставшихся 20% была резко снижена.
"Разработка однодозной терапии гонореи невероятно важна", - сказал Кейлер. "В некоторых случаях бактерии могут развить устойчивость к препарату, когда дополнительные дозы пропускаются, например, когда пациент начинает чувствовать себя лучше и перестает принимать антибиотики". С помощью одноразовой терапии пациент может завершить лечение после первого визита к своему врачу".
Чтобы лучше определить, как соединение ингибирует транс-трансляционный механизм, использовалась криоэлектронная микроскопия для получения изображений высокого разрешения соединения, поскольку оно связывается с бактериальной рибосомой.
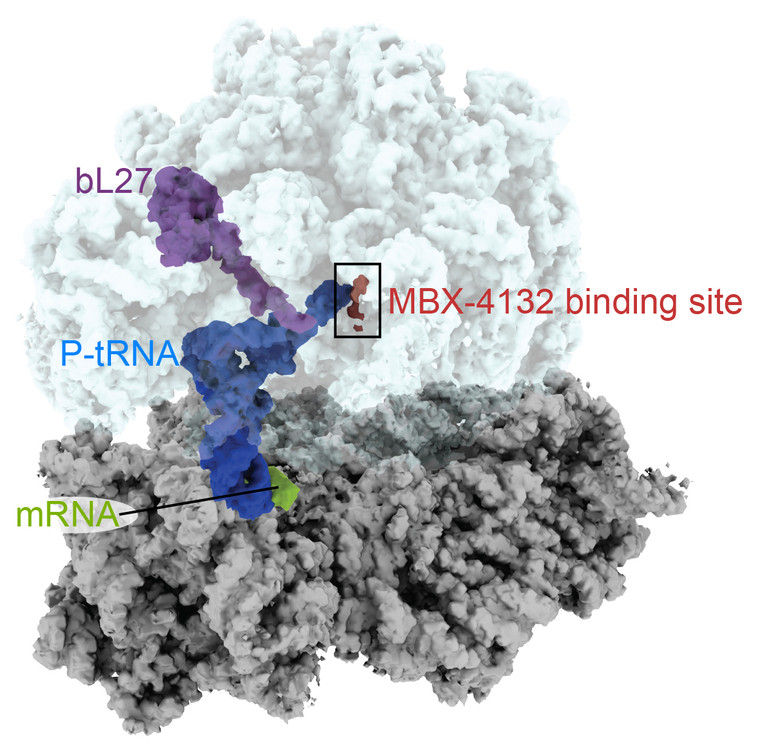
MBX-4132, связывается с рибосомой бактерий и вытесняет область белка (bL27, фиолетовый), которая является критической для транс-трансляционного пути у бактерий. Изображение: DUNHAM LAB, EMORY UNIVERSITY
"Дериватив MBX-4132 связывается с местом на рибосоме, которое отличается от всех известных мест связывания антибиотиков", - говорит Кейлер. "Новый препарат также вытесняет область рибосомального белка, которая, как мы думаем, может быть важна в ходе нормального процесса транс-трансляции. Поскольку транс-трансляция происходит только у бактерий, а не у человека, мы надеемся, что вероятность возникновения соединения, влияющего на синтез белка у человека, значительно снижается, и это гипотеза, в значительной степени подкреплена исследованиями безопасности и селективности, проведенными Microbiotix".
Исследовательская группа планирует провести дальнейшую оптимизацию состава перед проведением доклинических испытаний.
"Этот тип соединения на самом деле является ингибитором широкого спектра", - отметил Кейлер. Он эффективен против большинства грамположительных бактерий, включая туберкулез и трудно поддающиеся лечению стафилококковые инфекции (MRSA), а также некоторых грамотрицательных бактерий, и может стать перспективным кандидатом для будущей терапии. В данном исследовании мы закладываем основу для применения этого типа соединений и демонстрируем, что ингибирование транс-трансляционного механизма у бактерий является жизнеспособной антибактериальной стратегией".