Медицинский колледж штата Пенсильвания сообщает о двух случаях деструктивного детского менингита, связанного с инфекцией Paenibacillus.
Сообщения из Уганды впервые связали эти микроорганизмы с разрушительными неонатальными инфекциями, включая случаи аномального накопления спинномозговой жидкости, судорог и обширных повреждений головного мозга. С тех пор подобные случаи были зарегистрированы во многих штатах США, и обычные схемы лечения детей антибиотиками при бактериемии и менингите могут оказаться неэффективными, если речь идет о Paenibacillus. Микроорганизмы, относящиеся к этому роду, обычно идентифицируются как часть почвенного микробиома. Исторически считалось, что это редкий патоген для человека, но растущее число случаев заболевания новорожденных начало менять это представление.
В исследовании "Paenibacillus dendritiformis как причина деструктивного менингита у младенцев", опубликованном в журнале NEJM Evidence, авторы описали двух новорожденных с разрушительными неврологическими проявлениями, связанными с инфекцией, вызванной Paenibacillus, а также результаты лабораторных исследований, которые позволили идентифицировать организм на видовом уровне.
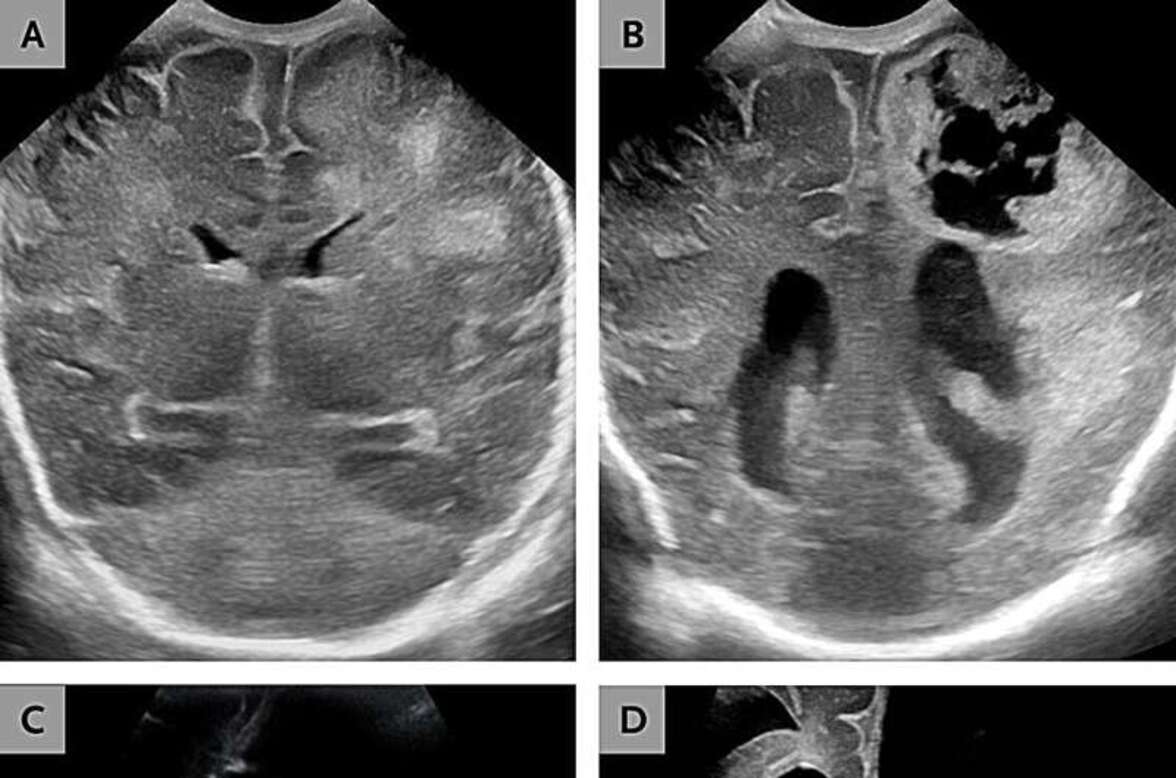
В одном случае речь шла о двухмесячной девочке, родившейся на сроке беременности 26 недель. В посевах крови и спинномозговой жидкости были обнаружены бактерии Paenibacillus thiaminolyticus, но никаких других патогенов обнаружено не было. Томография головного мозга выявила прогрессирующую гидроцефалию, энцефаломаляцию и образование абсцессов, что потребовало установки шунта.
Меропенем вводился в виде непрерывной инфузии в течение 8 недель. Затем были добавлены ванкомицин и рифампицин в связи с сохраняющимися нарушениями в циркуляции спинномозговой жидкости. Прием добавок с тиамином начался через четыре дня после появления симптомов, чтобы компенсировать ферментативное разрушение бактериями тиамина, истощение которого может привести к повреждению тканей головного мозга. В возрасте 8 месяцев неврологические функции оставались значительно нарушенными, при этом сохранялся зрительный контакт и улыбка, но неспособность есть перорально, сидеть без поддержки или переворачиваться самостоятельно.
Второй новорожденный появился на свет в возрасте 37 дней после преждевременных родов на сроке 33 недели беременности. Сложности с кормлением и отсутствие реакции привели к госпитализации. В посевах крови и спинномозговой жидкости снова были обнаружены P. thiaminolyticus, а на снимках был выявлен разжижающий менингоэнцефалит, при котором ткань мозга начинает превращаться в вязкую жидкость. Терапия включала внутривенное введение ампициллина и установку шунта. Клиническое ухудшение прогрессировало до трудностей с кормлением и судорог, кульминацией которых стала смерть в возрасте 11 месяцев.
При первоначальном лабораторном обследовании у обоих младенцев были ошибочно выявлены Paenibacillus thiaminolyticus, однако последующее полногеномное секвенирование изолятов подтвердило, что в обоих случаях это Paenibacillus dendritiformis. Виды Paenibacillus представляют дополнительные трудности для диагностики на микроскопическом уровне. Геномный анализ выявил множество признаков, связанных с патогенностью и устойчивостью к противомикробным препаратам. Идентифицированные гены кодируют оперон пилуса IV типа, несколько β-лактамаз, детерминанты устойчивости к ванкомицину и тиаминазу. Предыдущие данные предполагали, что пилус IV типа является фактором вирулентности при пенибактериозе новорожденных.
Оптимальная антимикробная терапия этих инфекций остается неопределенной. Секвенирование всего генома выявило в изолятах множество генов β-лактамаз. Геномное выявление детерминант устойчивости к ванкомицину представляет собой еще один уровень сложности. Хотя гены резистентности к ванкомицину также были обнаружены у изолятов из Уганды, американские штаммы были протестированы как фенотипически чувствительные к ванкомицину, что изначально наводило клиницистов на мысль о том, что лечение может быть эффективным. В этом случае любая резистентность может быть выявлена только при проведении полногеномного анализа или при отсутствии ответа на лечение.
В случаях, связанных с более благоприятными исходами, применялся меропенем в сочетании с добавками тиамина. Ферменты, разрушающие тиамин, вырабатываемые как P. thiaminolyticus, так и P. dendritiformis, являются биологически вероятным путем, связывающим инфекцию с неврологическими нарушениями. Недостаток тиамина в тканях головного мозга может способствовать разрушению тканей наряду с прямым микробиологическим воздействием.
Оба описанных младенца родились недоношенными и нуждались в интенсивной терапии новорожденных. Во многих случаях в США предполагались экологические факторы, включая почву и водные источники, но это объяснение представляется маловероятным. Прошлые наблюдения в Уганде выявили связь между количеством осадков и близостью к крупным водоемам, хотя применимость этого метода к условиям США остается неопределенной.
Данная бактериальная инфекция представляет собой клинически значимую и потенциально малоизученную причину серьезных неврологических нарушений, требующую повышенного внимания врачей, ухаживающих за младенцами раннего возраста. Антибиотикотерапия, обычно применяемая при неонатальной бактериемии и менингите, может не обеспечить адекватных контрмер. Раннее выявление, более широкое применение антимикробных препаратов и своевременная консультация нейрохирурга - все это имеет решающее значение для улучшения результатов лечения.