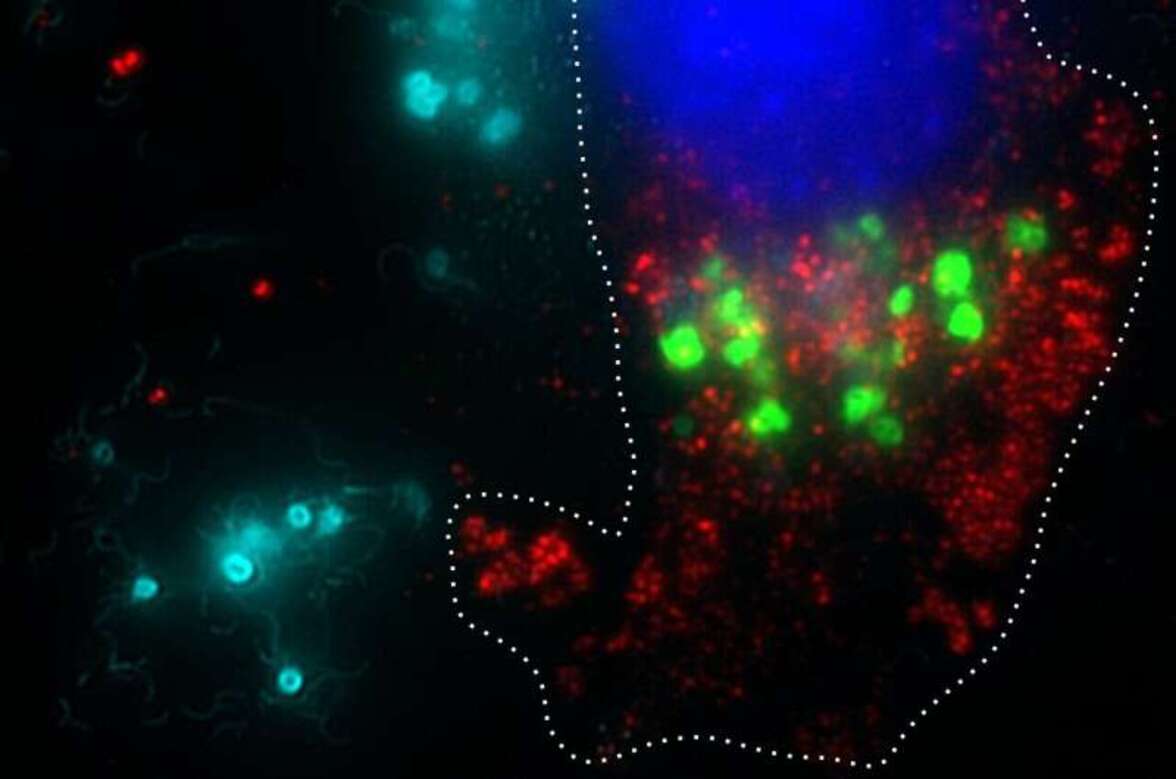
Для эффективного воздействия на внутриклеточные пути в раковых опухолях необходима система, которая бы специфически доставлялась в опухоли и интернализовалась в раковые клетки.
Группа ученых из Университета Массачусетса добилась впечатляющих успехов в разработке нетоксичной бактериальной терапии для доставки противораковых препаратов (протеолитический фермент каспаза-3) непосредственно в опухоли. Эта новая технология обещает стать безопасным и более эффективным методом лечения раковых заболеваний с высоким уровнем смертности, включая рак печени, яичников и метастатический рак молочной железы.
Клинические испытания с участием пациентов с раком начнутся в 2027 году. «Это замечательно, потому что теперь у нас есть все критические элементы для создания эффективного бактериального лечения рака», - рассказывает Нил Форбс, старший автор исследования, опубликованного недавно в журнале Molecular Therapy. «Мы пытаемся раскрыть потенциал лечения рака на поздних стадия. Бактерии естественным образом поселяются в опухолях и поскольку это лечение настолько целенаправленное, оно может воздействовать на некоторые виды рака без тяжелых побочных эффектов, которые наблюдаются при использовании других системных методов лечения, таких как химиотерапия».
Новые результаты стали кульминацией более чем десятилетних исследований, ранее группа занималась разработкой нетоксичных, генетически модифицированных штаммов сальмонеллы, способных воздействовать на опухоли и контролировать выделение противораковых препаратов внутри раковых клеток. Помимо того, что здоровые ткани не повреждаются, эта платформа для лечения рака способна доставить на порядки больше терапевтических препаратов, чем введенная доза, поскольку простые в изготовлении бактерии растут в опухолях по экспоненте. «Мы сосредоточились на том, как сделать этот штамм сальмонелл действительно безопасным и удобным для использования», - говорит Форбс. «Предпринятые нами шаги в области генной инженерии сделали этот штамм по меньшей мере в 100 раз безопаснее, чем все, что было опробовано в прошлом».
В этом штамме третьего поколения авторы придумали способ контролировать момент, когда бактерия после внутривенного введения вторгается в раковые клетки и осуществляет терапию. Это значительно улучшило способность воздействовать на опухоли более высокими концентрациями препарата, а также сделало лечение гораздо более безопасным.
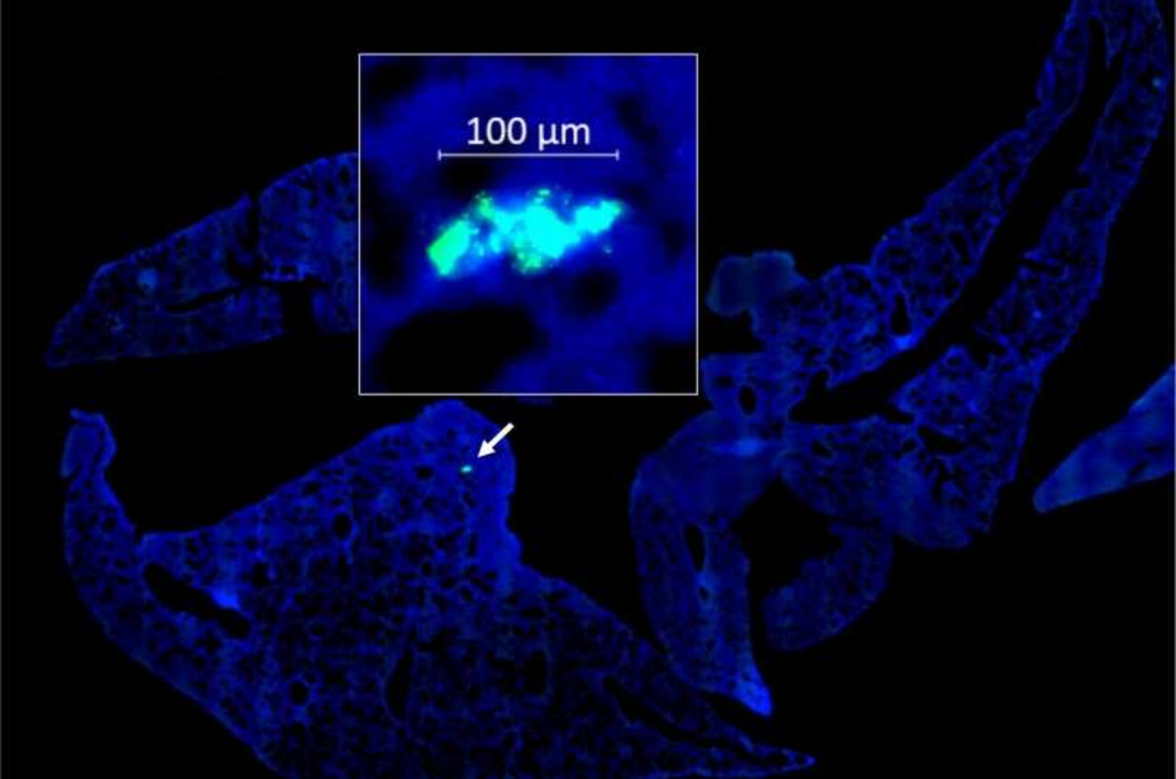
Метастатическая доставка: бактерия (зеленая, со стрелкой) находит и колонизирует метастатический узел рака молочной железы - размером с прядь волос в легком (синий). Фото: University of Massachusetts Amherst.
«В штамме первого поколения мы полагались на то, что бактерии сами найдут опухоль и проведут терапию. Но мы не могли контролировать, когда именно это происходит, поэтому существовали риски, связанные с вторжением в здоровые клетки, а также с преждевременным выведением бактерий из организма до того, как они колонизируют опухоли, и мы хотели снизить оба риска», - поясняет Форбс.
В самом начале исследования ученые обнаружили, что именно бактериальные жгутики, помогающие двигаться, позволяют бактериям вторгаться в раковые клетки. Поэтому они создали в бактериях генетически запрограммированную схему, которая включает производство жгутиков с помощью простой, безрецептурной дозы аспирина. Без «переключателя», обеспечиваемого салициловой кислотой, активным продуктом метаболизма в крови после приема аспирина, бактерии остаются в спящем состоянии в опухоли.
«Одна из основных составляющих этой технологии - контролируемая активация жгутиков», - объясняет Форбс. «Другая ключевая часть - когда бактерии попадают внутрь раковых клеток, мы создали для них схему самоуничтожения - они самостоятельно разрушаются когда доставляют терапию внутрь раковой клетки». Созданный клинически готовый штамм колонизировал метастатическую ткань молочной железы в 280 и 800 раз больше, чем окружающие здоровые ткани в легком и печени, соответственно. Точно контролируя колонизацию опухоли и инвазию клеток, этот штамм преодолевает критические ограничения бактериальной терапии и позволит лечить многие трудноизлечимые виды рака.
В доклинических исследованиях на мышиных моделях бактерии вводятся внутривенно. «Бактерии распространяются повсюду, но затем иммунная система быстро очищает ослабленные бактерии из тканей здоровых органов в течение двух дней. В течение этого времени бактерии продолжают экспоненциально расти только в опухолях. На третий день мы даем безрецептурную дозу аспирина, чтобы спровоцировать бактерии на вторжение в раковые клетки, за счет чего осуществляется терапия», - говорит Форбс. «Мы хотели сделать все как можно проще», - добавляет он. «Пациент может получить инфузию, а через три дня, дома, просто принять пероральную дозу аспирина».
Сейчас группа сосредоточена на организации процесса получения разрешения регулирующих органов для начала клинических испытаний. «Мы наблюдаем большой рост в области лечения рака с помощью микроорганизмов, - отмечает Форбс, - и мы гордимся тем, что находимся в авангарде этой области».