Все организмы - от бактерий до млекопитающих - обладают способностью эволюционировать и приспосабливаться к окружающей среде.
Но вирусы - это великие «оборотни», способные к мутации больше, чем любой другой организм. В результате они могут избегать воздействия препаратов или приобретать устойчивость к некогда эффективным противовирусным средствам. Исследование, проведенное учеными Гарвардской медицинской школы на примере вируса простого герпеса (HSV), проливает свет на один из способов, с помощью которого вирус становится устойчивым к лечению. Эта проблема может быть особенно сложной для людей с ослабленным иммунитетом, в том числе для тех, кто получает иммуносупрессивное лечение, и тех, кто родился с иммунодефицитом.
Используя сложный метод визуализации, называемый криогенной электронной микроскопией (крио-ЭМ), исследователи обнаружили, что то, как части белка, отвечающего за вирусную репликацию, перемещаются в различные позиции, может изменить восприимчивость вируса к лекарствам. Результаты исследования, опубликованные 27 августа в журнале Cell, отвечают на давние вопросы о том, почему некоторые вирусы, но не другие, восприимчивы к противовирусным препаратам и как вирусы становятся неуязвимыми для лекарств. Полученные результаты могут стать основой для разработки новых подходов, препятствующих способности вирусов опережать эффективные методы лечения.
Исследователям давно известно, что изменения, происходящие на тех участках вируса, где с ним связываются противовирусные препараты, могут сделать его устойчивым к терапии. Однако авторы нового исследования обнаружили, что, к их удивлению, в случае с HSV этого часто не происходит. Вместо этого они установили, что белковые мутации, связанные с устойчивостью к лекарствам, часто возникают далеко от места действия препарата. Эти мутации связаны с изменениями, которые меняют движение вирусного белка, или фермента, позволяющего вирусу реплицироваться. Это дает основания полагать, что использование лекарств, блокирующих конформационные изменения этих вирусных белков, может стать успешной стратегией преодоления лекарственной устойчивости. «Наши результаты показывают, что мы должны думать не только о типичных местах связывания лекарств», - считает старший автор исследования Джонатан Абрахам. «Это действительно помогает нам увидеть устойчивость к препаратам в новом свете».
Новые данные способствуют пониманию того, как изменения в конформации вирусного белка - или изменения в том, как различные части внутри этого белка перемещаются, когда он выполняет свою функцию - подпитывают устойчивость к лекарствам, и могут иметь значение для понимания эффективности лекарств и устойчивости к ним других вирусов, отмечают исследователи. Вирус HSV, от которого страдают миллиарды людей по всему миру, наиболее известен как причина "лихорадки на губах", но он также может привести к серьезным глазным инфекциям, воспалению мозга и повреждению печени у людей с ослабленным иммунитетом. Кроме того, HSV может передаваться от матери к ребенку через родовой канал во время родов и вызывать опасные для жизни неонатальные инфекции.
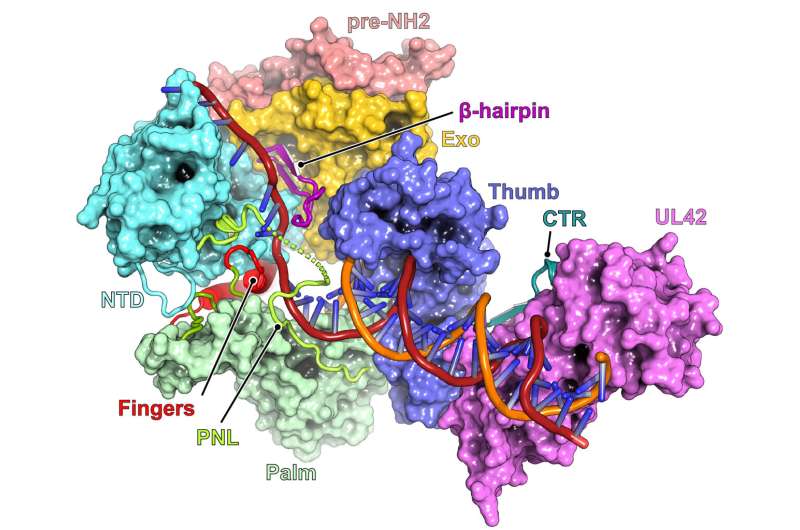
Вирус не может реплицироваться сам по себе. Для этого вирусы должны попасть в клетку хозяина, где они запускают свои инструменты репликации - белки, называемые полимеразами, чтобы создать свои копии. В данном исследовании изучался один из таких белков - вирусная ДНК-полимераза, имеющая решающее значение для способности HSV к самовоспроизведению и распространению. Способность выполнять свои функции обусловлена строением ДНК-полимеразы, которую часто сравнивают с рукой, состоящей из трех частей: ладони, большого пальца и остальных пальцев, каждый из которых выполняет критически важные функции.
Учитывая их роль в обеспечении репликации, эти полимеразы являются важнейшими мишенями для противовирусных препаратов, цель которых - остановить размножение вируса и распространение инфекции. Полимераза HSV является мишенью ацикловира, ведущего противовирусного препарата для лечения инфекции HSV, и фоскарнета, препарата второго ряда, применяемого при лекарственно-устойчивых инфекциях. Оба препарата действуют на вирусную полимеразу, но делают это по-разному.
Ученые долгое время пытались понять, как изменения в полимеразе делают вирус невосприимчивым к обычным дозам противовирусных препаратов и, в более широком смысле, почему ацикловир и фоскарнет не всегда эффективны против измененных форм полимеразы HSV. «За прошедшие годы были определены структуры многих полимераз из различных организмов, но мы до сих пор не до конца понимаем, что делает одни полимеразы, а не другие, восприимчивыми к определенным лекарствам», - говорит Абрахам. «Наше исследование показывает, что движение различных частей полимераз, известное как их конформационная динамика, является критическим компонентом их относительной восприимчивости к лекарствам».
Белки, включая полимеразы, не являются жесткими и неподвижными объектами. Напротив, они гибкие и динамичные. Состоящие из аминокислот, они изначально складываются в устойчивую трехмерную форму, известную как нативная конформация - их базовая структура. Но в результате действия различных сил сцепления и диспергирования различные части белков могут перемещаться при контакте с другими клеточными компонентами, а также под воздействием внешних факторов, таких как изменение pH или температуры. Например, "пальцы" белка-полимеразы могут раскрываться и сжиматься, как и пальцы руки.
Конформационная динамика - способность различных частей белка двигаться - позволяет им эффективно выполнять множество важнейших функций при ограниченном количестве компонентов. Лучшее понимание конформационной динамики полимераз - это недостающее звено между структурой и функциями, включая то, реагирует ли белок на лекарство и может ли он стать устойчивым к нему в будущем. Многие структурные исследования позволили запечатлеть ДНК-полимеразы в различных конформациях. Однако детальное понимание влияния конформационной динамики полимеразы на устойчивость к лекарствам отсутствует.
Чтобы решить эту задачу, исследователи провели серию экспериментов, сосредоточившись на двух распространенных конформациях полимеразы - открытой и закрытой, - чтобы определить, как каждая из них влияет на восприимчивость к лекарствам. С помощью крио-ЭМ они провели структурный анализ, чтобы получить визуализацию атомных структур полимеразы HSV с высоким разрешением в различных конформациях, а также при связывании с противовирусными препаратами ацикловиром и фоскарнетом. Структуры, ассоциированные с лекарствами, показали, как эти два препарата избирательно связывают полимеразы, которые охотнее принимают одну конформацию, чем другую. Один из препаратов, фоскарнет, действует, захватывая "пальцы" ДНК-полимеразы так, что они застревают в так называемой закрытой конфигурации.
Кроме того, структурный анализ в сочетании с вычислительным моделированием показал, что несколько мутаций, удаленных от мест связывания лекарства, придают противовирусную устойчивость, изменяя положение "пальцев" полимеразы, ответственных за закрытие лекарства для остановки репликации ДНК. Это открытие стало неожиданным поворотом. До сих пор ученые считали, что полимеразы частично закрываются только при присоединении к ДНК и полностью закрываются только при добавлении строительного блока ДНК - дезоксинуклеотида. Однако оказалось, что полимераза HSV может полностью закрыться, просто находясь рядом с ДНК. Таким образом, ацикловиру и фоскарнету проще зацепиться за полимеразу и остановить ее работу, тем самым прекратив вирусную репликацию.
«Я работал над изучением полимеразы HSV и устойчивости к ацикловиру в течение 45 лет. Тогда я думал, что мутации устойчивости помогут нам понять, как полимераза распознает особенности природных молекул, которые имитируют лекарства», - делится еще один соавтор исследования Дональд Коэн, профессор биологической химии и молекулярной фармакологии. «Я рад, что эта работа показывает, что я ошибался, и наконец-то дает нам хотя бы одно четкое объяснение, почему полимераза HSV избирательно ингибируется препаратом».