Быстрое восстановление является отличительной особенностью Т-клеток памяти. В то время как наивным клеткам требуются дни для формирования эффекторных ответов на новые угрозы, клетки памяти, имеющие опыт взаимодействия с антигеном, начинают продуцировать цитокины уже через несколько часов после повторного контакта.
Исследователи из Детского медицинского центра Цинциннати (США) выяснили, как определенные иммунные клетки на молекулярном уровне запрограммированы на более быструю реакцию, когда организм сталкивается с уже известной угрозой, что позволяет понять природу иммунной памяти и ее связь с такими заболеваниями, как астма, рассеянный склероз и воспалительные заболевания кишечника. В исследовании, опубликованном в журнале Cell Reports, было установлено, что ДНК «памяти» CD4⁺ Т-клеток — иммунных клеток, образующихся после перенесенной инфекции или вакцинации, — запрограммирована на активацию ключевых генов защиты в течение нескольких часов. В отличие от них, наивным Т-клеткам, впервые сталкивающимся с патогеном, может потребоваться несколько дней, чтобы организовать ответ. Разница заключается в эпигеноме клеток — химических и структурных особенностях, которые определяют, насколько легко гены могут включаться.
«Хотя феномен быстрого восстановления иммунной памяти хорошо известен, лежащие в его основе механизмы изучены недостаточно», — объясняет старший автор исследования Эмили Миральди. «В данном исследовании мы использовали геномику единичных клеток и моделирование сетей регуляции генов, чтобы точно определить факторы транскрипции, которые связываются с ДНК, чтобы поддерживать клетки памяти в готовности к быстрой и мощной иммунной защите».
Используя передовые методы анализа единичных клеток, исследователи изучили десятки тысяч человеческих CD4⁺ Т-клеток от четырех доноров, отслеживая активность генов и доступность хроматина — показатель того, насколько открытыми являются регуляторные участки ДНК — до и после активации. Авторы обнаружили, что многие регуляторные области, контролирующие гены иммунного ответа, уже доступны в покоящихся Т-клетках памяти, что дает им преимущество при повторном появлении известного патогена. «Клетки памяти не начинают с одной и той же отправной точки», — пояснила Миральди. «Многие из регуляторных областей, контролирующих быстрые иммунные реакции, уже открыты в покоящихся клетках памяти».
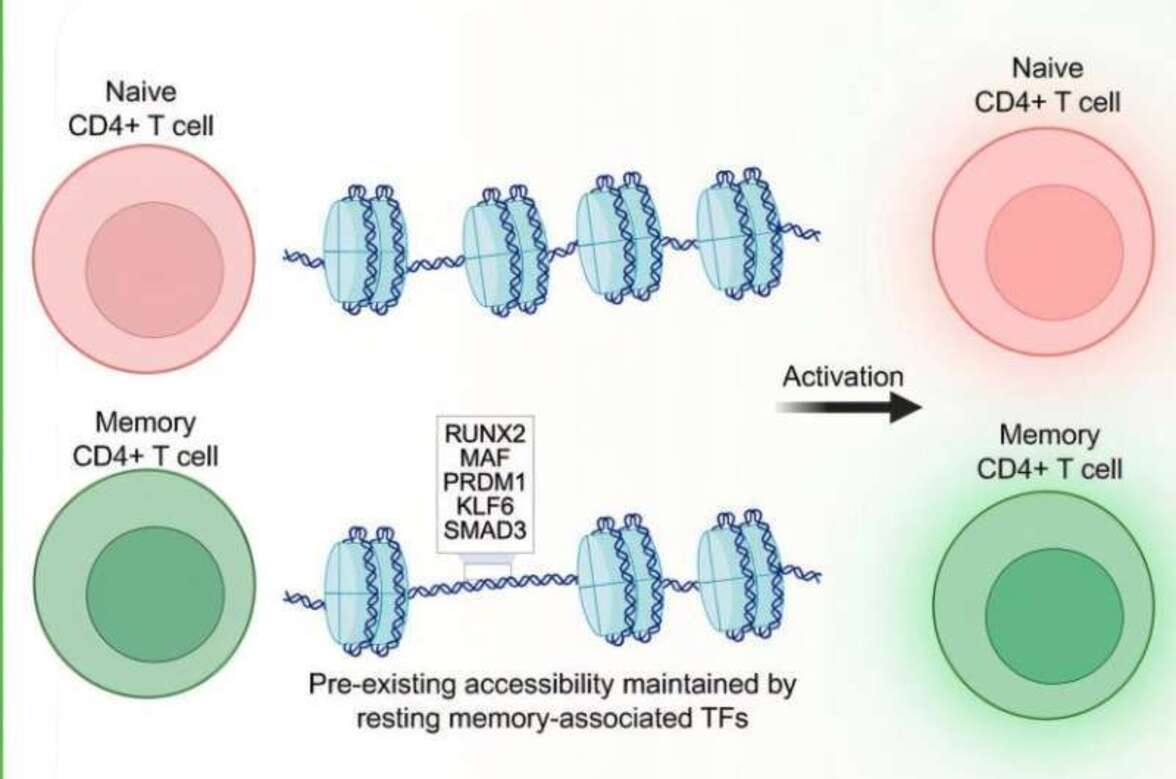
В ходе исследования было выявлено пять факторов транскрипции — белков, контролирующих активность генов, — которые последовательно отличают Т-клетки памяти от наивных клеток. К ним относятся факторы KLF6, MAF, PRDM1, RUNX2 и SMAD3. Вместе эти регуляторы образуют основную сеть, которая поддерживает готовность иммунной системы в течение длительных периодов покоя и стимулирует быструю активацию во время реакций восстановления памяти. «Эта работа выводит нас за пределы изучения отдельных генов», — отметила Миральди. «Она показывает, как сети регуляторов взаимодействуют для управления иммунной памятью».
Исследователи построили математическую модель этих регуляторных сетей и проверили ее с помощью данных более 100 дополнительных участников, а также образцов от людей, проходящих пероральную иммунотерапию против аллергии на арахис. Затем они сопоставили модель с данными крупных генетических исследований и обнаружили, что многие варианты ДНК, связанные с астмой, аллергическими и аутоиммунными заболеваниями, находятся в регуляторных областях, специфичных для иммунной памяти. Эти варианты не изменяют сами белки. Вместо этого они, по-видимому, влияют на то, насколько быстро или сильно активируются гены иммунного ответа, что потенциально может способствовать гиперактивным или плохо контролируемым иммунным реакциям.
Полученные результаты могут помочь в будущих усилиях по разработке вакцин, обеспечивающих более быструю или сильную иммунную защиту, например, для пожилых людей, которые часто не реагируют достаточно активно на стандартные вакцины. Между тем, эти результаты могут помочь ученым разработать методы лечения, которые более точно нацелены на вредные иммунные реакции, не подавляя иммунитет в целом. «Это дает нам системную карту того, как поддерживается иммунная память, — сказала Миральди. — Эта основа может помочь нам лучше понять — и в конечном итоге лучше контролировать — иммунные реакции в норме и при заболеваниях».