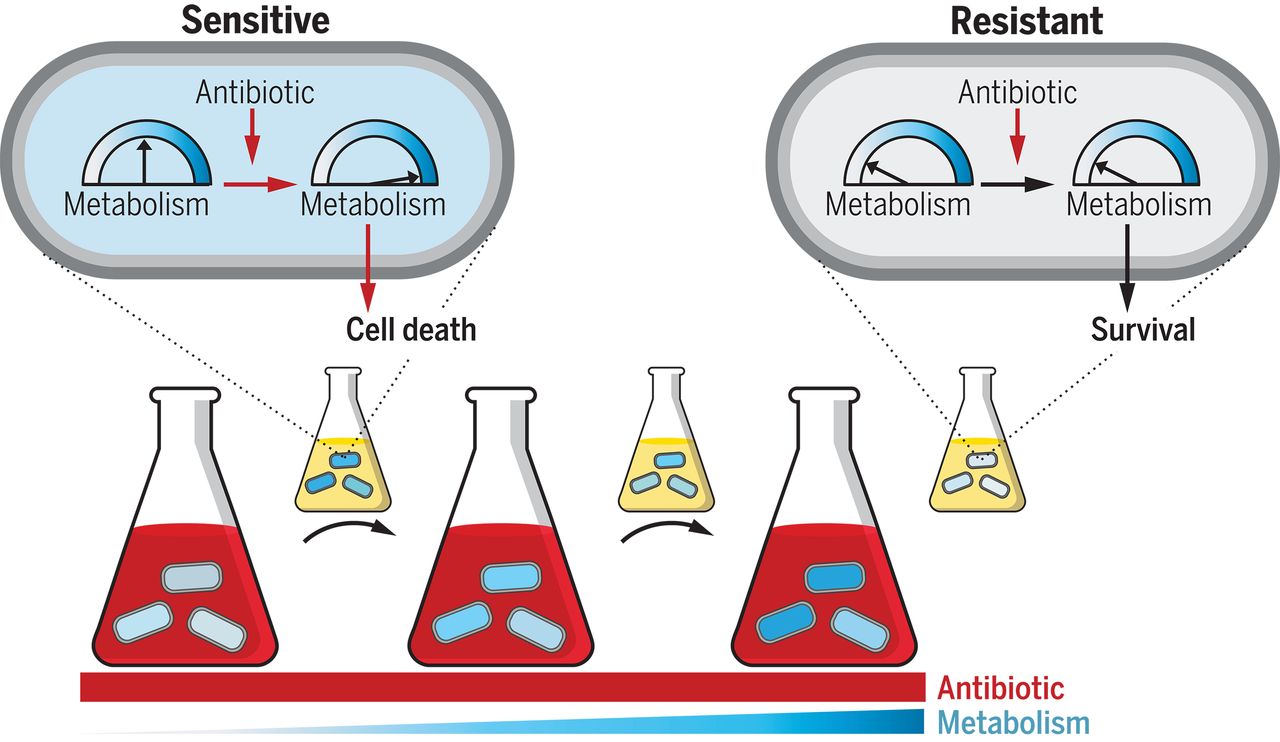
Исследования показывают, что принуждение бактерий тратить больше энергии может сделать их более чувствительными к антибиотикам.
Большинство мутаций, которые порождают резистентность, происходят в генах на которые нацелен тот или иной антибиотик. Другие мутации позволяют бактериям разрушать антибиотики или выкачивать их через клеточные мембраны.
В настоящее время исследователи MIT определили еще один класс мутаций, которые помогают бактериям развивать резистентность. На модели E. coli они обнаружили, что мутации в генах, участвующих в метаболизме, также могут помочь бактериям избежать токсического воздействия различных антибиотиков. Полученные результаты проливают свет на фундаментальные основы действия антибиотиков и предлагают потенциальные новые пути разработки лекарственных средств, которые могли бы повысить эффективность существующих антибиотиков.
"Это исследование дает нам представление о том, как мы можем повысить эффективность существующих антибиотиков, поскольку оно акцентирует внимание на том, что метаболизм бактерий играет важную роль. В частности, наша работа указывает на то, что эффективность антибиотиков может быть повышена, если можно усилить метаболический ответ патогена", - говорит Джеймс Коллинз, старший автор исследования, опубликованного в Science.
Новое исследование основано на предыдущей работе лаборатории Коллинза, которая показала, что при лечении антибиотиками многие бактерии вынуждены наращивать свой метаболизм, что приводит к накоплению побочных токсичных продуктов. Эти побочные продукты повреждают клетки и способствуют их гибели.
Однако, несмотря на роль гиперактивного метаболизма в гибели клеток, ученые не обнаружили никаких доказательств того, что такое метаболическое давление приводит к мутациям, которые помогают бактериям уклоняться от лекарств. Исследователи отправились на поиски таких мутаций.
Во-первых, они провели исследование, аналогичное обычно используемому для поиска мутаций резистентности к антибиотикам. В этом типе скрининга, известном как адаптивная эволюция, исследователи начинают с лабораторного штамма кишечной палочки, а затем обрабатывают клетки постепенно увеличивающимися дозами того или иного антибиотика. Затем исследователи секвенируют геномы клеток, чтобы увидеть, какие виды мутаций возникли в ходе обработки. Ранее такой подход не приводил к мутациям генов, участвующих в метаболизме, из-за ограничений по количеству генов, которые можно было бы секвенировать.
"Многие из исследований, проводившихся ранее, рассматривали несколько клонов, эволюционировавших поодиночке, или же они секвенировали, возможно, пару генов, в которых ожидали увидеть мутации, потому что они связаны с тем, как действует антибиотик", - говорит Коллинз. "Это дает нам очень точную картину этих генов резистентности, но ограничивает наш взгляд на все остальное".
Например, ципрофлоксацин нацелен на ДНК-гиразу, фермент, участвующий в репликации ДНК, и заставляет этот фермент повреждать клеточную ДНК. При обработке ципрофлоксацином в клетках часто развиваются мутации в гене ДНК-гиразы, что позволяет им уклоняться от этого механизма.
При первом скрининге адаптивной эволюции ученые проанализировали больше E. coli и гораздо больше генов, чем было изучено ранее. Это позволило им выявить мутации в 24 метаболических генах, в том числе генах, связанные с метаболизмом аминокислот и углеродным циклом - совокупностью химических реакций, позволяющих клеткам извлекать энергию из сахара, высвобождая углекислый газ в качестве побочного продукта.
Чтобы определить еще больше мутаций, связанных с метаболизмом, исследователи запустили второй скрининг, в котором заставили клетки перейти в усиленное метаболическое состояние. В этих исследованиях кишечную палочку ежедневно обрабатывали высокой концентрацией антибиотика при постепенном повышении температуры. Температурные изменения постепенно переводили клетки в очень активное метаболическое состояние, и в то же время они также постепенно вырабатывали резистентность к препарату.
Затем исследователи секвенировали геномы этих бактерий и обнаружили некоторые из тех же мутаций, связанных с метаболизмом, которые они видели при первом скрининге, плюс дополнительные мутации в генах метаболизма. К ним, помимо генов углеродного цикла, относились гены, участвующие в синтезе аминокислот, особенно глутамата. Затем они сравнили свои результаты с библиотекой геномов резистентных бактерий, выделенных от пациентов, и обнаружили многие из тех же мутаций.
Затем они осуществили некоторые из этих мутаций в типовых штаммах E. coli и обнаружили, что скорость их клеточного дыхания была значительно снижена. Когда они обрабатывали эти клетки антибиотиками, для уничтожения бактерий требовались гораздо большие дозы. Это говорит о том, что, выключив метаболизм после воздействия антибиотиков, бактерии могут прекратить образование вредных побочных продуктов.
Полученные данные повышают вероятность того, что принуждение бактерий к повышенному метаболическому состоянию может повысить эффективность существующих антибиотиков, говорят исследователи. Теперь они планируют продолжить изучение того, как эти метаболические мутации помогают бактериям уклоняться от использования антибиотиков, в надежде найти более конкретные мишени для новых вспомогательных препаратов.