Инфекции, связанные с оказанием медицинской помощи (ИСМП), представляют собой серьезную проблему для здоровья пациентов, медицинских работников и посетителей медицинских учреждений.
По оценкам Всемирной организации здравоохранения, у каждого десятого пациента развивается ИСМП, а только в больницах США ИСМП являются причиной 1,7 миллиона инфекций и 99 000 связанных с ними смертей в год.
Среди этих инфекций более трети вызваны Enterobacteriaceae, семейством бактерий, включающим наиболее распространенные патогенные для человека виды и ведущие причины нозокомиальных инфекций, такие как Escherichia coli, Salmonella enterica и Klebsiella pneumoniae. Учитывая, что эти инфекции приобретаются в среде с высоким давлением антимикробных препаратов, они часто вызываются бактериями с резистентностью к антимикробным препаратам (AMR) и множественной лекарственной устойчивостью (MDR). За последние 2 десятилетия резко возросло число инфекций, вызванных энтеробактериями с MDR, особенно с ростом числа энтеробактерий, продуцирующих карбапенемазу. Эти патогены способны противостоять не только действию всех доступных бета-лактамов (кроме азтреонама), но и других доступных классов антимикробных препаратов, таких как фторхинолоны и аминогликозиды, что оставляет врачам мало вариантов лечения. Это приводит к удорожанию лечения, увеличению продолжительности пребывания в стационаре, повышению риска осложнений и смертности.
Постоянный рост числа этих патогенов в медицинских учреждениях обусловлен многими факторами, основными из которых являются их способность распространяться и персистировать в окружающей среде и бессимптомно в организме пациентов, а также медицинских работников и персонала. Риск колонизации, последующего инфицирования и смертности от Enterobacteriaceae экспоненциально возрастает с возрастом, историей болезни и длительностью пребывания в больнице.
Колонизация может быть определена как бессимптомное присутствие патогена в организме человека. Она является первым шагом к заболеванию колонизированного пациента, с большей или меньшей степенью тяжести, а также одним из основных факторов, способствующих вспышкам инфекций в медицинских учреждениях. Действительно, некоторые исследования показали, что от 36 до 39% пациентов, колонизированных AMR Enterobacteriaceae, впоследствии заболевают. Бессимптомная колонизация, особенно бактериями с MDR, представляет собой серьезную проблему для общественного здравоохранения, поскольку возбудитель, который несет колонизированный пациент, может случайно передаться другим пациентам, которые могут заразиться, что приведет к увеличению риска осложнений и даже смерти.
Программы профилактики и контроля инфекций (ППК) обеспечивают критически важные меры по предотвращению передачи заболеваний в медицинских учреждениях, способные снизить уровень ИСМП по меньшей мере на 30%, что иногда является единственным решением для профилактики и предотвращения колонизации и инфекций с MDR.
Используя доступность масштабных данных о здравоохранении, которые регулярно собираются и хранятся в электронных медицинских картах (ЭМК), были предложены модели машинного обучения для раннего выявления пациентов с риском инфицирования и поддержки программ ППК. Классические методы машинного обучения, такие как "деревья решений" и "рандомный лес", продемонстрировали хорошую эффективность для прогнозирования пациентов, подверженных риску ИСМП.
Для метициллин-резистентного золотистого стафилококка и Clostridioides difficile было показано, что эти алгоритмы могут предупреждать уже за 5 дней до постановки диагноза. Методы машинного обучения для прогнозирования колонизации были также изучены в недавних исследованиях. Древовидные методы машинного обучения, такие как "деревья решений", "рандомный лес" и "экстремальный градиентный бустинг", достигли чувствительности и специфичности выше 80% для выявления видов MDR из различных патогенных семейств, а использование пространственно-временных признаков для выявления пациентов, колонизированных ванкомицин-резистентным энтерококком, позволило получить площадь под кривой приемной операционной характеристики (AUROC) выше 88%.
Хотя классические модели машинного обучения и созданные вручную характеристики могут показывать эффективные результаты в ограниченных случаях использования, они часто не могут обобщить крупномасштабные и долговременные данные ЭМК. Еще одним ограничением предыдущих подходов к прогнозированию колонизации Enterobacteriaceae является игнорирование ключевых взаимодействий между пациентами и медицинскими работниками, что препятствует их применению в сложных сетях медицинского обслуживания.
Для устранения этих недостатков мы предлагаем подход с глубинным обучением, основанный на архитектуре графовой нейронной сети (ГНС). Этот подход направлен на учет взаимодействия между пациентами и медицинскими работниками в палатах и вне их, а также других клинических и пространственно-временных характеристик для прогнозирования риска колонизации Enterobacteriaceae у стационарных пациентов. Наши модели были обучены и оценены с помощью базы данных Medical Information Mart for Intensive Care (MIMIC-III) и сравнены с классическими базовыми моделями машинного обучения. Интересно отметить, что модели ГНС обеспечивают более высокую прогностическую эффективность для раннего выявления чувствительных к антимикробным препаратам (AMS), AMR и MDR Enterobacteriaceae по сравнению с базовыми моделями, обученными с использованием информации о сети пациентов или без нее.
Наш основной вклад можно суммировать следующим образом:
- Мы предлагаем модель колонизации на основе графов, которая учитывает пространственно-временные характеристики в дополнение к демографическим и клиническим характеристикам. Чтобы избежать погрешностей в модели из-за утечки информации, мы не используем информацию о противомикробных препаратах.
- Мы разрабатываем ГНС-модели для прогнозирования колонизации, которые изучают паттерны сетей передачи на основе пространственно-временных данных и данных о пациентах. Предлагаются и оцениваются различные конфигурации сети и пути передачи.
- Мы оцениваем нашу модель в сравнении с классическими современными базовыми моделями машинного обучения и показываем, что она достигает превосходной производительности как при доступе базовых моделей к информации о сети через внедрение node2vec, так и без него. Мы также проводим исследование объяснимости, чтобы продемонстрировать способность модели автоматически определять признаки, связанные с факторами риска колонизации.
- Существует множество исследований, посвященных прогнозированию ИСМП. Насколько нам известно, это первая попытка исследовать проблему прогнозирования риска колонизации Enterobacteriaceae с помощью ГНС и предоставить гипотезу передачи, основанную на данных.
Методы:
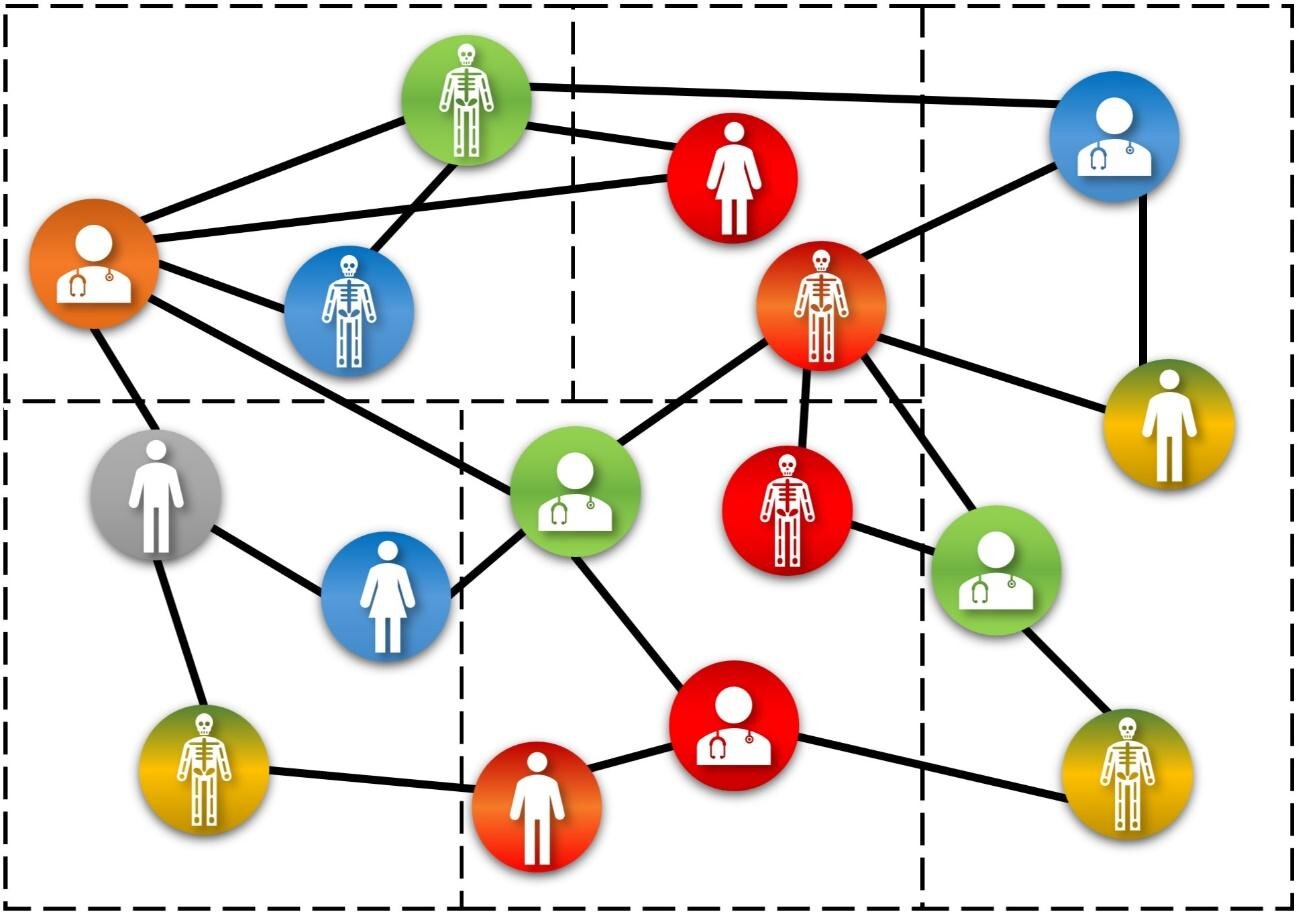
Прогнозирование колонизации было определено как бинарная задача, цель которой - предсказать, будет ли пациент колонизирован MDR Enterobacteriaceae в нежелательной части тела во время пребывания в больнице. Для учета топологических особенностей взаимодействие между пациентами и медицинскими работниками моделировалось с помощью графовой структуры, где пациенты описываются узлами, а их взаимодействие - гранями. Затем была обучена модель графовой нейронной сети (ГНС) для изучения паттернов колонизации из сети пациентов, обогащенной клиническими и пространственно-временными характеристиками.
Результаты:
Модель ГНС достигла эффективности 0,91 и 0,96 площади под кривой операционной характеристики приемника (AUROC) при обучении в индуктивном и трансдуктивном режимах, соответственно, что на 8 % выше базового показателя логистической регрессии (0,88). При сравнении топологий сети конфигурация, учитывающая грани, связанные с палатой (0,91 индуктивная, 0,96 трансдуктивная), превосходит конфигурации, учитывающие грани, связанные с ухаживающими лицами (0,88, 0,89), и оба типа граней (0,90, 0,94). Для 3 наиболее распространенных энтеробактерий с MDR AUROC варьируется от 0,94 для Citrobacter freundii до 0,98 для Enterobacter cloacae при использовании модели ГНС с наилучшими показателями.
Выводы:
Топологические признаки с помощью графового моделирования улучшают производительность моделей машинного обучения для прогнозирования колонизации Enterobacteriaceae. ГНС могут быть использованы для поддержки программ профилактики и контроля инфекций для выявления пациентов, подверженных риску колонизации MDR Enterobacteriaceae и другими семействами бактерий.