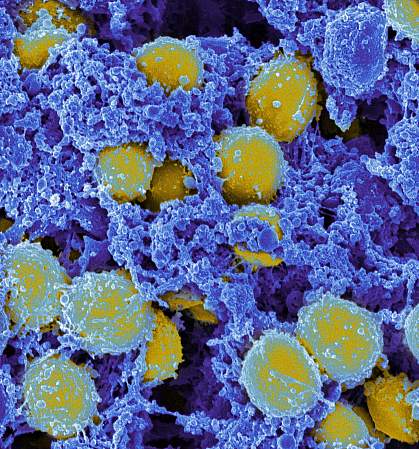
Staphylococcus aureus является одной из ведущих причин смертности от инфекций во всем мире, представляя собой единственный бактериальный патоген, кроме Mycobacterium tuberculosis, число смертей от которого постоянно превышает один миллион в год.
Большинство тяжелых инфекций, вызванных S.aureus, происходит в больничных условиях, часто у предрасположенных пациентов, таких как люди с ослабленным иммунитетом или перенесшие операцию.Большинство таких инфекций - это инфекции нижних дыхательных путей, крови, брюшины или внутрибрюшной полости. Кроме того, S.aureus является распространенным источником легких и умеренных инфекций кожи. У некоторых людей инфекции кожи, вызванные S.aureus, могут быть хроническими или рецидивирующими. Более того, S.aureus был вовлечен в развитие атопического дерматита (экземы).
Поразительное разнообразие типов инфекций, которые может вызывать S.aureus, во многом объясняется большим количеством различных факторов и механизмов вирулентности этого возбудителя. Эти факторы и механизмы включают молекулы адгезии для инфицирования тканей, очень большое количество механизмов иммунной агрессии для борьбы практически со всеми аспектами врожденной защиты хозяина, и, что самое печальное, ряд агрессивных токсинов, которые лизируют многие иммунные и другие типы клеток.
Единственным общепринятым методом лечения тяжелых инфекций, вызванных S.aureus, является антибиотикотерапия. Однако S.aureus стал резистентным к различным антибиотикам, наиболее ярким примером чего является метициллин-резистентный S.aureus (MRSA). Ситуация усугубляется тем, что, несмотря на значительные усилия исследователей, по прежнему не удается разработать эффективную вакцину или альтернативные методы лечения, такие как препараты, направленные на борьбу с вирулентностью.
S.aureus является бессимптомным колонизатором на эпителиальных и слизистых поверхностях человека и многие исследования показали, что инфекция S.aureus коррелирует с колонизацией и происходит от колонизирующих штаммов. Поэтому деколонизация является часто предлагаемым и реализуемым подходом для профилактики инфекции S.aureus. Однако эффективность существующих процедур остается спорной. В этом обзоре мы даем описание процесса колонизации S.aureus и обсуждаем меры по деколонизации с акцентом на то, как последние исследования могут стимулировать новые подходы.
Колонизация S.aureus
S.aureus колонизирует человеческое тело, отдавая предпочтение определенным областям, в первую очередь кишечнику, носу, некоторым участкам кожи (паху и подмышечным впадинам), а также глотке и влагалищу. S.aureus колонизирует только некоторых людей, причем частота колонизации носа и кишечника колеблется от одной пятой до одной трети населения, а частота колонизации других областей несколько ниже и более изменчива. От 1% до 3% людей могут быть колонизированы MRSA.
Могут также существовать географические и социально-экономические различия в частоте колонизации. Частота колонизации (культуральная позитивность) выше у новорожденных и детей, чем у взрослых. Высокие показатели колонизации среди населения, составляющие около 70% после рождения, снижаются до 20-30% в первые несколько месяцев жизни и далее падают примерно до 10-20% в возрасте 1-2 лет. Для кишечной колонизации эта тенденция к снижению в течение первых нескольких месяцев жизни также отражается в снижении числа колонизирующих S.aureus у носителей.
Уровень назальной колонизации снова возрастает примерно до 10 лет (∼50%), после чего этот показатель снижается примерно до 20-30% у взрослых, что является сходным для назальной и кишечной колонизации. Во многих исследованиях проводится различие между постоянной и временной колонизацией, при этом постоянная колонизация обычно определяется при наличии двух положительных образцов с интервалом между ними не менее 1 недели ("культуральное правило"). Хотя колонизации на разных участках тела обычно коррелируют, только временная колонизация на определенном участке может быть обусловлена скрытой локализацией S.aureus на другом участке и объяснять тот факт, что после местной деколонизации люди часто повторно колонизируются тем же штаммом. Следует отметить, что как носители, так и не носители S.aureus имеют высокие концентрации антистафилококковых антител в сыворотке крови, что указывает на то, что большинство людей хотя бы в какой-то момент своей жизни контактировали с S.aureus.
Колонизация S.aureus обычно оценивается только качественно. В количественных исследованиях колониеобразующие единицы (КОЕ) в носовой полости варьировали от 102 до 106 КОЕ на мазок, при этом наиболее часто сообщалось о среднем значении в диапазоне 104-105. Только в нескольких исследованиях определялись КОЕ в фекалиях в качестве косвенного показателя колонизации кишечника, при этом сообщалось о примерно 106-107 КОЕ на 100 г фекалий - среднем весе человеческого стула. По оценкам одного из недавних исследований, количество S.aureus в кишечнике примерно на три порядка выше, чем в носу. Количество колоний S.aureus даже на участках кожи чаще всего обсемененных S.aureus (подмышечные впадины и пах), ничтожно мало.
Примечательно, что ни одни из имеющихся на сегодняшний день данных, включая данные об однонуклеотидных полиморфизмах хозяина и бактериальной интерференции, рассмотренные ниже, не объясняют удовлетворительно почему S.aureus колонизирует одних людей, но не других. Частота колонизации S.aureus в популяции может быть гораздо выше, чем предполагалось ранее, но часто остается незамеченной, поскольку колонизация S.aureus эпителия кишечника может быть оценена только косвенно, путем анализа фекалий, а колонизация эпителия носа - путем анализа мазков, что потенциально дает много ложноотрицательных результатов. Кроме того, носовая полость часто остается единственным местом для исследования.
Колонизация полости носа
Традиционно колонизация S.aureus преимущественно ассоциируется с полостью носа. Постоянная колонизация носа встречается примерно у 20% (диапазон 12-30%) людей, а примерно 30% являются периодическими носителями (диапазон 16-70%). Уровень колонизации в преддверии и полости носа одинаков, и примерно 5% S.aureus могут быть внутриклеточными. Считается, что колонизация носа S.aureus определяется взаимодействием с защитными силами организма и специфическими генами бактерий. Некоторые однонуклеотидные полиморфизмы в генах хозяина, в том числе в IL-4, C-реактивном белке, Toll-подобных рецепторах, и дефенсинах, были связаны с частотой колонизации S.aureus, но эти различия незначительны, и значительной наследственности колонизации S.aureus не выявлено.
Факторы S.aureus, которые ассоциируются с колонизацией, включают тейхоевые кислоты, которые связываются с эпителием носа через рецептор, экспрессируемый эпителиальными клетками (SREC-1), и поверхностные белки, такие как фактор B, которые связываются через цитокератин 10. Вопрос о том, способствует ли образование биопленки колонизации носа, является спорным. Колонизация глотки тесно связана с колонизацией носа, однако показатели колонизации глотки могут несколько отличаться и даже превышать показатели колонизации полости носа.
Кишечная колонизация
Кишечнику как месту колонизации S.aureus уделяется не так много внимания, как носу. Однако вышеупомянутое сравнение КОЕ носового мазка и фекалий позволяет предположить, что кишечник, а не нос, является первичным местом колонизации S.aureus и даже может служить резервуаром, из которого пополняются другие места колонизации. В подтверждение этой идеи было показано, что по сравнению с колонизацией только носовой полости наличие колонизации как носовой, так и кишечной полости связано с повышенной частотой положительных кожных культур. Более того, в клиническом исследовании вмешательство, направленное исключительно на кишечник, значительно уменьшило количество S.aureus в кишечнике при одновременном снижении количества S.aureus в полости носа.
Многие вопросы о колонизации кишечника S.aureus остаются без ответа. Например, точная область в кишечнике, где колонизируется S.aureus, неизвестна. В мышиных моделях S.aureus, по-видимому, связан со слоем слизи. Кроме того, остается неизвестным, колонизируют ли одни и те же штаммы нос и кишечник. Только в одном исследовании сообщалось, что нос и кожа прямой кишки носителей были колонизированы различными штаммами по меньшей мере в 40% случаев.
Механизмы кишечной колонизации S.aureus до сих пор плохо изучены. Было показано, что поверхностные структуры S.aureus, включая капсулу, тейхоевые кислоты и поверхностный белок фактор A, влияют на колонизацию кишечника у мышей. У детей наличие нескольких генов поверхностных белков, например генов, кодирующих коллаген-связывающий белок (Cna) и фибронектин-связывающий белок (FnbA), было связано с колонизацией кишечника. Зависимость прикрепления к кишечному эпителию от поверхностных белков предполагает прямое взаимодействие с эпителием, несмотря на наличие слизи. Учитывая скудность сообщений о способности S.aureus разрушать слизь, механизм, лежащий в основе этого процесса, неясен; колонизация кишечника (и носа) S.aureus может происходить в местах с пониженным содержанием слизи. Кроме того, сообщалось, что колонизация кишечника сильно зависит от системы кворум сенсинга (Agr), которая контролирует экспрессию большинства факторов вирулентности S.aureus и влияет на фенотипы, связанные с вирулентностью, такие как воспаление, уклонение от иммунитета и образование биопленок; однако конкретные факторы, регулируемые Agr, лежащие в основе колонизации кишечника, остаются неустановленными.
Колонизация кожи
S.aureus обычно отсутствует на здоровой коже человека или имеет очень низкую концентрацию на коже; несколько более высокая концентрация наблюдается только во влажных областях, таких как подмышечные впадины и пах. S.aureus на коже в основном изучался с точки зрения кожных заболеваний и факторы, способствующие бессимптомной колонизации остаются неизученными. В дополнение к своей роли контролера экспрессии дельта-токсина при атопическом дерматите, Agr может иметь значение для колонизации кожи, хотя этот эффект был показан только в моделях с воспалением, таких как модели атопического дерматита.
Колонизация и инфекция
Несмотря на то, что S.aureus считается частью микробиоты здорового человека и колонизация S.aureus обычно протекает бессимптомно, он может вызывать широкий спектр инфекций. В ряде исследований было установлено, что около 80% инфекционных изолятов клонально соответствуют колонизационным изолятам того же пациента, что указывает на колонизацию как источник инфекции, и что люди, являющиеся носителями S.aureus, подвержены повышенному риску развития инфекций, вызванных S.aureus. Например, колонизация носовой полости S.aureus коррелирует с последующей бактериемией, а также связана с обострением таких редких заболеваний, как гранулематоз Вегенера.
Кроме того, S.aureus является наиболее распространенной причиной инфекций хирургических участков, которые развиваются в результате попадания колонизирующих бактерий во время операции. Более того, у пациентов с колонизацией S.aureus частота инфекций выше, чем у пациентов без колонизации им, в группах пациентов с повышенной колонизацией S.aureus, таких как пациенты, проходящие диализ. Наконец, инфекции MRSA связывают со статусом колонизации как в обществе, так и в стационаре, и группы пациентов с известной повышенной колонизацией MRSA, такие как пациенты учреждений длительного ухода, чаще заболевают инфекциями MRSA.
Хотя в большинстве исследований анализировалась только корреляция между колонизацией носа и инфекциями, в некоторых исследованиях также анализировалась корреляция с колонизацией кишечника или прямой кишки. Так, у детей с абсцессами S.aureus значительно чаще выделялся из прямой кишки, но не из носа, чем в контрольной группе; кишечная колонизация S.aureus ассоциировалась с повышенной частотой положительных кожных культур; а у людей с ректальной и назальной колонизацией риск инфицирования S.aureus был выше, чем у тех, кто имел только назальную колонизацию.
Колонизация S.aureus и инфекция имеют сложную и многофакторную взаимосвязь, которая еще не до конца изучена. Заметная корреляция колонизации с риском инфекции вызывает вопросы о том, существуют ли специфические молекулярные детерминанты, которые необходимы для того, чтобы S.aureus стал инвазивным. Несмотря на четкую ассоциацию генетических вариаций с инфекцией и типами инфекции, некоторые исследования показали, что инвазивные линии не отличаются от тех, которые колонизируют нос или кишечник. Этот вывод может указывать на то, что в целом генетический репертуар S.aureus, необходимый для колонизации и инфекции, схож или что восприимчивость хозяина играет более решающую роль, или и то и другое.
Однако в процессе развития инфекции S.aureus может происходить генетическая адаптация, влияние которой на переход от комменсального к патогенному образу жизни должно быть изучено более подробно. Например, любые мутации, происходящие в Agr и делающие его дисфункциональным, увеличивают образование биопленок и успешность ассоциированной с устройствами и хронической костной инфекции, а также связаны с персистирующей бактериемией. Это наблюдение противоречит продемонстрированной роли Agr при колонизации и других видах инфекции.
Если говорить о восприимчивости хозяина, то было обнаружено несколько факторов риска, повышающих вероятность инфицирования S.aureus, включая иммуносупрессию, хронические заболевания, такие как диабет или хроническая обструктивная болезнь легких, а также редкие генетические нарушения, такие как хроническая гранулематозная болезнь. Исследования геномных ассоциаций не могли выявить факторы хозяина в значительной степени определяющие восприимчивость к инфекции S.aureus у здоровых людей и пока не было обнаружено, что однонуклеотидные полиморфизмы в области HLA класса II ассоциированы с инфекцией S.aureus. Вопрос о том определяют ли специфические наследственные генетические признаки колонизацию остается малоизученным. Датское исследование близнецов не выявило существенной роли генетики хозяина в колонизации полости носа S.aureus. Наконец, колонизация S.aureus может предрасполагать человека к последующим инфекциям S.aureus, приучая иммунную систему толерантно относиться к антигенам S.aureus; однако эти вопросы до сих пор изучены слабо.
Традиционные методы деколонизации
В связи с распространением резистентности к противомикробным препаратам возрос интерес к разработке мер по деколонизации S.aureus. Были оценены пероральные антибиотики для деколонизации S.aureus, иногда в сочетании с местными антибиотиками или антисептиками. Несмотря на то, что пероральные антибиотики могут принести пользу некоторым группам пациентов, эти антибиотики не следует назначать для деколонизации здоровым людям из-за риска развития антибиотикорезистентности и неизбежного разрушения здорового микробиома кишечника.
Основное внимание в исследованиях уделялось коже и полости носа. Для деколонизации носовой полости обычно используются антибиотики местного действия, такие как мупироцин, а для деколонизации кожи - антибиотики или антисептики местного действия, такие как хлоргексидин. Для деколонизации носовой полости и кожи, а иногда и таких областей, как влагалище, часто сочетают подходы на основе антибиотиков и антисептиков. Следует отметить, что деколонизация на основе антибиотиков или антисептиков считается целесообразной только для тех групп пациентов, которые подвергаются риску инфицирования лишь в течение короткого периода времени, например, для тех, кто собирается подвергнуться хирургическому вмешательству. Поскольку пациенты обычно реколонизируются в течение нескольких недель после деколонизации, что предшествует общему восстановлению микробиома, длительное воздействие антибиотиков и антисептиков не рекомендуется из-за соображений развития резистентности к ним и их вредного воздействия на кожу, которое включает устойчивое нарушение микробиоты.
Применение антибиотиков
Мупироцин, ингибитор бактериальной изолейцин-тРНК-лигазы, долгое время был антибиотиком выбора для местной деколонизации S.aureus. Несколько исследований показали, что мупироцин действует быстро и эффективно снижает колонизацию S.aureus в носовой полости или на коже, хотя мупироцин следует применять многократно в течение 5 дней. Долгосрочные исследования эффективности показали, что первоначальное очищение эффективно в течение нескольких недель, но реколонизация в течение 3 месяцев является обычным явлением. Примечательно, что назальное применение только мупироциновой мази не приводит к деколонизации экстраназальных участков.
Однако использование антибиотиков для деколонизации также имеет ряд недостатков, наиболее важным из которых является развитие резистентности и разрушение микробиоты в местах применения антибиотика. Разрушение микробиоты очень опасно, поскольку не позволяет полезным микробам, сдерживающим размножение патогенов, оказывать свое действие. Что касается развития резистентности, то повторные или длительные курсы применения мупироцина могут вызвать значительное повышение резистентности к S.aureus или другим патогенам, поэтому такого использования следует избегать.
Применение антисептиков
Обычно для деколонизации S.aureus используются такие антисептики, как хлоргексидин, который разрушает мембраны, и повидон-йод (PI), йодофор, активность которого обусловлена выделением йода. Местная деколонизация кожи на основе хлоргексидина доказала свою эффективность в снижении инфекции как у хирургических, так и у нехирургических пациентов и обычно сочетается с деколонизацией носа. Было показано, что PI снижает количество назальных метициллин-чувствительных S.aureus и MRSA у пациентов, перенесших операцию, и здоровых добровольцев.
В недавнем исследовании, PI однако, уступал мупироцину по способности производить деколонизацию носовой полости. Использование антисептиков для деколонизации также имеет свои недостатки. К ним относится возможность раздражения кожи или аллергических реакций, что может ограничить их использование, особенно при многократном применении. Кроме того, как и антибиотики, антисептики могут нарушить естественную микробиоту, что может привести к чрезмерному росту условно-патогенных микроорганизмов.
Испытания процедур деколонизации
Было проведено множество клинических испытаний и ретроспективных анализов для оценки влияния процедур деколонизации S.aureus на профилактику инфекций. Из этого списка были исключены исследования, включавшие системные пероральные антибиотики, в связи с вышеуказанными опасностями, связанными с ними. В большинстве исследований использовались или оценивались процедуры деколонизации с помощью назального мупироцина, иногда в сочетании с хлоргексидином или PI-ваннами, гигиеническими салфетками или душем.
В испытании REDUCE-MRSA универсальный подход оказался более эффективным, чем целевой подход (направленный на носителей MRSA после скрининга) или подход, предусматривающий только изоляцию и скрининг, в обоих случаях в плане снижения количества MRSA-положительных культур и инфекций кровотока. Однако выраженного влияния процедур деколонизации на профилактику именно MRSA-инфекций кровотока не было.
Хотя это исследование проводилось на пациентах отделения интенсивной терапии, в недавнем исследовании ABATE не было отмечено существенного снижения уровня колонизации MRSA или инфекций кровотока у пациентов, не относящихся к отделениям интенсивной терапии. В исследовании CLEAR, проведенном после выписки, деколонизация и гигиеническое обучение были на 30% эффективнее в профилактике MRSA-инфекции в течение 1 года, чем только гигиеническое обучение. В большинстве испытаний сообщалось о сходных результатах, а также о значительном эффекте деколонизации у пациентов в отделении интенсивной терапии.
В недавнем исследовании, проведенном в домах престарелых, колонизация MRSA и риск перевода в стационар по всем причинам и в связи с инфекциями были существенно снижены благодаря всеобщей деколонизации.
В целом, внедрение мер по деколонизации S.aureus было успешным, что, скорее всего, способствовало снижению числа инфекций, связанных с оказанием медицинской помощи, которое наблюдается, например, в США. Тем не менее, безусловно, есть возможности для совершенствования. Основные остающиеся проблемы связаны с низкой эффективностью мер по деколонизации, реколонизацией и жестким характером деколонизирующих агентов. Кроме того, исследования по секвенированию целых геномов указывают на важность учета разнообразия штаммов для деколонизации.
Новые методы деколонизации
В настоящее время разрабатывается несколько новых и перспективных методов деколонизации S.aureus у людей, которые позволяют избежать пагубного воздействия на микробиом, связанного с использованием антибиотиков и антисептиков. В некоторых методах используются бактериоцины местного применения, обладающие активностью против S.aureus. В модели колонизации носовой полости хлопковой крысы бактериоцин эпидермицин NI01 из S.epidermidis так же эффективно снижал колонизацию S.aureus, как и мупироцин. В испытаниях на людях бактериоцины Bacillus subtilis, наносимые на кожу пациентов с акне, снижали численность S.aureus на коже и уменьшали поражение кожи акне. Однако другие бактериоцины, включая бацитрацин, уступали мупироцину в исследованиях по деколонизации людей.
Хотя использование бактериоцинов представляет собой повышение специфичности по сравнению с использованием антибиотиков широкого спектра действия, бактериоцины по-прежнему имеют широкий целевой спектр и, таким образом, потенциально могут оказывать значительное влияние на состав микробиома. Лизины, полученные из фагов или бактерий, более специфичны. В мышиной модели кожной инфекции лизин, специфичный для S.aureus, снижал колонизацию кожи эффективнее, чем мупироцин. Кроме того, однократное применение крема с лизостафином уничтожило MRSA в носовой полости хлопковых крыс.
Также изучалось применение целых фагов. В исследовании на мышах применение двух стафилококковых фагов уничтожило S.aureus в полости носа более эффективно, чем применение мупироцина. Однако в другом исследовании применение комбинации из двух фагов не привело к существенному снижению количества MRSA в модели колонизации носовой полости поросят. Пока нет результатов испытаний на людях по использованию фагов или лизинов для деколонизации S.aureus, что является предметом дальнейших исследований, как и использование фагов для лечения инфекций.
Другие недавно реализованные подходы основаны на использовании пробиотических бактерий, которые способны ограничить колонизацию S.aureus, конкурируя за питательные вещества, модулируя иммунный ответ хозяина для создания более благоприятной среды для непатогенных бактерий, продуцируя антимикробные вещества, такие как бактериоцины, или вмешиваясь в механизмы колонизации S.aureus. Преимущество пробиотических бактерий в микробиоме - по крайней мере временное - заключается в длительном или даже постоянном продуцировании ингибирующих веществ или эффектов.
Конкуренция за питательные вещества и модулирование иммунного ответа хозяина с целью создания более благоприятной среды для непатогенных бактерий представляют собой довольно неспецифические способы, которые часто применяются при пероральном введении пробиотических бактерий и основаны на идее, что любая бактерия, которая находится в благоприятных отношениях с хозяином или в какой-то степени стимулирует защитные иммунные реакции, или и то и другое, снизит численность патогенов. Эти методы обычно малоэффективны. Кроме того, механизмы, лежащие в основе действия пробиотиков, остаются малоизученными. Например, в одном из исследований пероральное применение штамма Lactobacillus rhamnosus снизило колонизацию кишечника S.aureus на 15%, но не оказало никакого влияния на другие участки тела.
Несколько штаммов, продуцирующих бактериоцины, в основном коагулазоотрицательные стафилококки, были использованы для снижения колонизации S.aureus в доклинических исследованиях. Большинство штаммов были найдены в результате анализа и скрининга микробиома человека. Например, анализ назальных изолятов привел к открытию штамма Staphylococcus lugdunensis, который вырабатывал ранее не идентифицированное вещество, названное лугдунином, которое подавляло рост S.aureus. Колонизация носа S.lugdunin-продуцирующим S.lugdunensis отрицательно коррелировала с колонизацией S.aureus, а совместное культивирование штамма, продуцирующего лугдунин, и S.aureus привело к небольшому снижению количества S.aureus, по сравнению с совместным культивированием изогенного лугдунин-отрицательного S.lugdunensis.
В другом исследовании при скрининге кожных изолятов был выделен штамм Staphylococcus hominis, который продуцировал бактериоцин микрококцин P1145 и значительно снижал колонизацию кожи S.aureus. Кроме того, в исследовании, посвященном атопическому дерматиту и включавшем модели мышей и испытания на людях, другой штамм S.hominis, продуцирующий два бактериоцина лантибиотического типа, уменьшил количество S.aureus на коже мышей и людей. Хотя применение штамма S.hominis не уменьшило симптомы атопического дерматита в испытаниях на людях, исследование показало, что в принципе продуценты бактериоцинов могут безопасно использоваться для уменьшения колонизации кожи S.aureus у людей.
Другой подход к снижению колонизации S.aureus пробиотическим способом с использованием живых бактерий основан на ингибировании кворум сенсинга. Этот подход не убивает S.aureus, но ограничивает его способность к колонизации, зависящую от Agr. Применение штамма Staphylococcus caprae, который продуцирует перекрестные ингибирующие аутоиндуцирующие пептиды, заметно ограничило рост MRSA в модели колонизации кожи мыши. В недавнем испытании на людях для уменьшения колонизации S.aureus использовалась выработка В.subtilis ингибирующих кворум липопептидов фенгицина. В этом плацебо-контролируемом исследовании пероральное употребление спор пробиотика B.subtilis уничтожило более 95% общего количества S.aureus, обитающих в организме человека, не влияя на кишечную микробиоту.
Выводы
Последние исследования колонизации S.aureus позволили лучше понять основные механизмы как S.aureus может взаимодействовать с другими членами микробиоты и как колонизация связана с инфекцией. Однако многое еще остается неясным. Например, механизмы взаимодействия внутри микробиоты только начинают раскрываться, и необходимы дальнейшие исследования, включающие также оценку их значимости in vivo. Кроме того, хотя известно, что в большинстве случаев инфекция, скорее всего, возникает в результате колонизации, механизм, лежащий в основе перехода от колонизации к инфекции, и какие факторы хозяина и потенциальные генетические полиморфизмы хозяина влияют на этот переход, остаются неизвестными. Более того, кишечная колонизация и динамика колонизации других мест колонизации требуют повышенного внимания.
Используемые в настоящее время стратегии деколонизации S.aureus для профилактики инфекций имеют успех, но, безусловно, могут быть усовершенствованы. Кроме того, в этих стратегиях обычно используются антибиотики, что является проблематичным в свете рационального использования антибиотиков. Новые подходы к преодолению пагубных последствий применения антибиотиков или антисептиков широкого спектра действия за счет использования более специфических веществ и пробиотиков, направленных против S.aureus, находятся в стадии доклинической, а в некоторых случаях уже клинической разработки. Кроме того, признание потенциальной ключевой роли кишечной колонизации S.aureus потребует изменения фокуса в отношении разработки стратегий деколонизации. Однако необходимы дальнейшие исследования для установления долгосрочной безопасности и эффективности этих новых стратегий деколонизации, чтобы они могли быть успешно внедрены в клиническую практику.