Разнообразные виды бактерий, населяющие кишечник человека и известные как микробиота кишечника, обеспечивают важные преимущества для здоровья.
Одним из ключевых преимуществ является колонизационная резистентность - способность ограничивать колонизацию кишечника патогенами, которые могут вызывать заболевания. Было обнаружено множество механизмов, влияющих на способность микробиоты обеспечивать колонизационную резистентность, но эти механизмы часто зависят от контекста и конкретных штаммов или видов бактерий. В результате мы не знаем общих принципов, позволяющих предсказать, какие сообщества микробиоты будут защитными, а какие позволят патогенам колонизироваться.
Используя экологический подход, мы изучили колонизационную резистентность симбионтов кишечника человека по отношению к двум важным бактериальным патогенам - Klebsiella pneumoniae и Salmonella enterica серовар Typhimurium. Мы изучали колонизационную резистентность симбионтов как по отдельности, так и в комбинациях с возрастающим разнообразием, чтобы выявить общие закономерности, лежащие в основе колонизационной резистентности, используя как анализы in vitro, так и эксперименты in vivo с гнотобиотическими мышами.
Результаты
Мы культивировали 100 симбионтов кишечника человека по отдельности с K. pneumoniae, а затем с S. Typhimurium и ранжировали симбионты по их способности обеспечивать колонизационную резистентность. Однако даже самые лучшие виды обеспечивали ограниченную защиту от патогенов в наших экспериментах. Напротив, когда мы объединяли виды в разнообразные сообщества, включающие до 50 видов, мы обнаружили случаи, когда рост патогенов был значительно ограничен. Та же картина наблюдалась и при колонизации безмикробных мышей подмножеством этих сообществ и заражении патогеном.
Таким образом, для колонизационной резистентности важно экологическое разнообразие, но мы также обнаружили, что важен и состав сообществ. Как in vitro, так и in vivo мы обнаружили, что колонизационная резистентность зависит от присутствия определенных видов, даже если эти виды сами по себе обеспечивают незначительную защиту. Мы смогли объяснить эти закономерности способностью некоторых сообществ блокировать рост патогена, потребляя питательные вещества, необходимые патогену.
Таким образом, блокированию питательных веществ способствует как разнообразие, так и присутствие определенных ключевых видов, которые увеличивают совпадение между потреблением питательных веществ сообществом и патогеном. Таким образом, включение ключевого вида, тесно связанного с патогеном, может стать главным фактором защиты сообществ, поскольку обеспечивает более высокую степень метаболического дублирования.
Однако одного этого, как правило, недостаточно. Мы обнаружили, что для обеспечения блокирования питательных веществ и, следовательно, колонизационной резистентности необходимо присутствие дополнительных, часто отдаленно родственных видов. Наконец, мы использовали принцип блокирования питательных веществ для предсказания in silico более защищенных и менее защищенных сообществ для нового штамма-мишени - клинического изолята Escherichia coli, резистентного к антимикробным препаратам. Затем мы экспериментально проверили колонизационную резистентность этих сообществ.
Эта работа показала, что мы можем успешно идентифицировать защитные сообщества из большого числа возможных комбинаций, используя как фенотипические показатели метаболического дублирования, так и более общие показатели геномного дублирования.
Заключение
Наши результаты подтверждают предположение о том, что более разнообразные микробиомы могут принести пользу здоровью, в частности, они могут улучшить защиту от колонизации патогенами. Мы также обнаружили, что колонизационная резистентность является коллективным свойством сообществ микробиома; другими словами, один штамм защищает только в сочетании с другими. Важно отметить, что хотя увеличение разнообразия микробиома повышает вероятность защиты от патогенов, ключевое значение имеет совпадение профилей использования питательных веществ сообществом и патогеном. Наша работа предлагает путь к оптимизации состава микробиомов для защиты от патогенов.
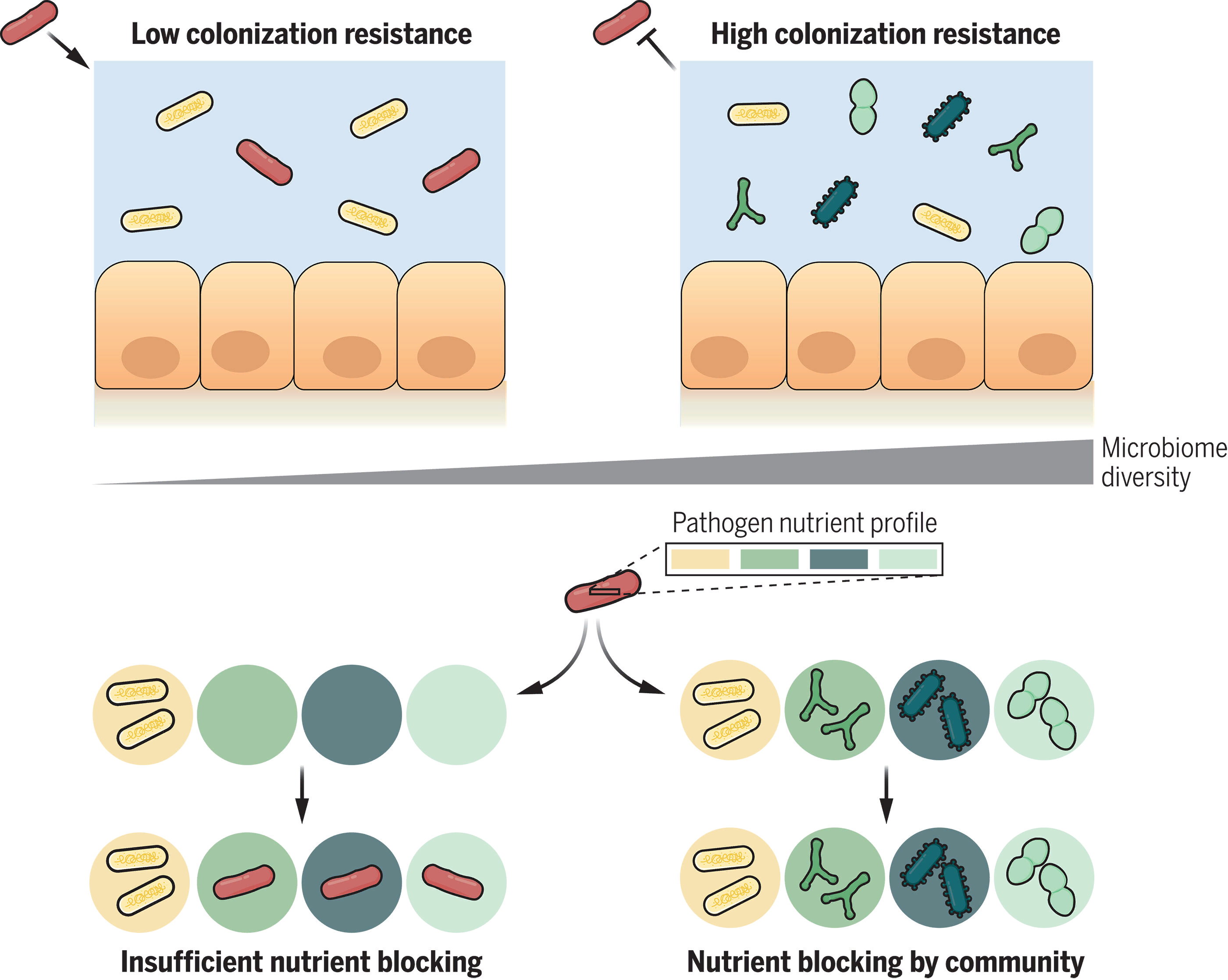
Патогены (красные) не могут колонизироваться, когда они совпадают с сообществом (желтые и зеленые бактерии) в профилях потребления питательных веществ (питательные ниши обозначены цветными кружками). По мере увеличения разнообразия микробиома возрастает вероятность потребления различных питательных веществ, что помогает блокировать рост патогенов и повышает колонизационную резистентность.