Когда речь идет о лечении бактериальных инфекций, одной из целей антимикробного управления является сокращение ненужного использования антибиотиков - но есть определенные сценарии, когда комбинированная антибактериальная терапия имеет важные преимущества.
Традиционное тестирование чувствительности к противомикробным препаратам (AST), однако, включает в себя тестирование одного противомикробного препарата против бактериального изолята, чтобы увидеть, подавляет ли он рост. Как же работает AST для комбинаций противомикробных препаратов?
Комбинированная антибактериальная терапия не является новой концепцией: Mycobacterium tuberculosis, одна из старейших известных бактериальных инфекций, должна лечиться несколькими препаратами, чтобы предотвратить возникновение резистентности во время терапии. Простые точечные мутации, с помощью которых туберкулезные палочки развивают резистентность к препаратам, используемым для их лечения, неизбежно происходят во время длительных курсов терапии, необходимых для лечения туберкулеза, так что один препарат, применяемый отдельно, быстро становится бесполезным. Однако вероятность того, что отдельная бацилла выработает резистентность к трем или четырем препаратам одновременно, исчезающе мала. Когда начинается лечение туберкулеза, врачи используют несколько препаратов, к которым чувствителен изолят пациента, по отдельности, чтобы предотвратить возникновение резистентности к любому из них.
Однако для большинства бактериальных патогенов развитие резистентности к широко используемым противомикробным препаратам - гораздо более сложный процесс, включающий возникновение многочисленных мутаций с течением времени или приобретение полностью сформированного элемента резистентности путем передачи плазмид, поэтому вероятность возникновения резистентности при монотерапии гораздо ниже. Но комбинированная терапия также имеет потенциальные преимущества, помимо предотвращения возникновения резистентности: второй препарат может усилить активность первого или подавить активность механизма резистентности.
Как узнать, когда два препарата лучше, чем один? В исследовательских лабораториях существует несколько различных способов проверки синергизма противомикробных препаратов. В действительности эти методы определяют не то, что два препарата лучше одного, а то, что два препарата при совместном применении оказывают эффект, превышающий сумму их индивидуальных действий - другими словами, два препарата вместе лучше двух по отдельности.
Одним из таких методов является метод "шахматной доски", который представляет собой двумерную адаптацию классического метода микроразведений в бульоне (ММБ). В этом методе бактериальная суспензия добавляется в лунки микротитровального планшета, в которые были добавлены 2 различных препарата в последовательных 2-кратных разведениях. Этот метод имеет существенные ограничения в воспроизводимости, связанные, в частности, с присущей тестированию ММБ вариабельностью, которая усугубляется, когда тестируются сразу 2 препарата, хотя стандартные определения, используемые для синергии в методе "шахматной доски", учитывают эту ожидаемую вариабельность.
Другим широко используемым методом является метод "тайм-килл", в котором количество колоний получают в последовательные временные точки из жидких культур, в которых бактерии подвергаются воздействию каждого антибиотика в отдельности и двух препаратов вместе. В отличие от шахматного метода, который может обнаружить ингибирование бактерий только в определенный момент времени, анализ "тайм-килл" дает информацию о гибели бактерий в течение определенного времени. (Следует отметить, что эти два метода не всегда совпадают, что подчеркивает необходимость разработки надежных, стандартизированных методов тестирования синергизма).
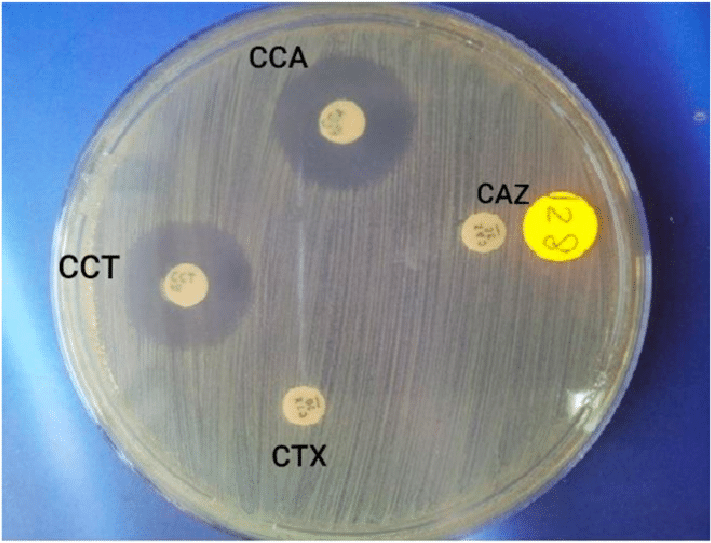
Интересно, однако, что ни один из этих методов не используется в лаборатории клинической микробиологии для тестирования бактериальных патогенов, выделенных от пациентов. (Некоторые референс-лаборатории предлагают синергетическое тестирование для грибов и микобактерий). Как же лаборатория клинической микробиологии помогает определить, будет ли комбинация препаратов полезной? Для некоторых фиксированных комбинированных препаратов лаборатории просто используют стандартные тесты на чувствительность к комбинации препаратов, чтобы определить, ингибируется ли изолят комбинацией. Это касается комбинаций β-лактамов/ингибиторов β-лактамазы, таких как амоксициллин-клавуланат или цефтазидим-авибактам. В большинстве случаев компонент этих комбинаций ингибиторов β-лактамазы (клавуланат или авибактам) по отдельности неэффективен, поэтому если изолят чувствителен к комбинации и устойчив только к β-лактамному препарату, то можно предположить синергизм.
Триметоприм-сульфаметоксазол - это широко используемый фиксированный комбинированный антибиотик, состоящий из двух ингибиторов синтеза фолатов, которые обладают повышенной активностью при совместном применении. Хотя бактериальный изолят может быть протестирован на чувствительность к каждому компоненту этой комбинации по отдельности, лаборатории обычно просто тестируют на чувствительность к комбинации триметоприма и сульфаметоксазола. Поскольку два компонента этой комбинации используются почти исключительно в комбинации, этого результата достаточно: врачам не нужно знать, является ли комбинация синергичной по отношению к своим компонентам, а просто знать, эффективна ли она против изолята, инфицировавшего их пациента.
Существует также особый случай "синергетического тестирования" аминогликозидов для видов Enterococcus. Правильно называемый тестом на выявление аминогликозидной резистентности высокого уровня (HLAR), на самом деле это вовсе не синергетический тест. Он включает в себя тестирование изолята энтерококка на чувствительность к очень высоким концентрациям гентамицина или стрептомицина - аминогликозидных антибиотиков, которые сами по себе обладают минимальной активностью против энтерококков. Однако при использовании в комбинации с некоторыми антибиотиками, действующими на клеточную стенку, аминогликозиды (в частности, гентамицин и стрептомицин) достигают высоких внутриклеточных концентраций, подобных тем, которые используются в тесте HLAR, и усиливают активность основного препарата. Таким образом, если изолят энтерококка отрицательно реагирует на HLAR, можно прогнозировать, что он ответит на комбинированную терапию аминогликозидами (ампициллин, пенициллин или ванкомицин плюс гентамицин или стрептомицин).
Еще один препарат, который используется почти исключительно в комбинации, - это рифампин, который часто добавляют к таким препаратам, как оксациллин или ванкомицин, для лечения эндокардита протезированного клапана.
Но кроме фиксированных комбинированных препаратов и нескольких классических примеров, приведенных выше, роль лаборатории в оказании помощи врачам в определении того, какие комбинации антибиотиков могут обладать повышенной активностью для их пациентов, в настоящее время очень ограничена. Используя описанные выше методы "шахматной доски" и "тайм-килл", исследования in vitro выявили множество различных комбинаций с потенциальной синергической активностью, особенно против патогенов с множественной лекарственной резистентностью, таких как карбапенем-резистентные Enterobacteriaceae (CRE). Возможно клиницисты захотят, чтобы лаборатория протестировала некоторые из этих комбинаций против изолята пациента, и будут разочарованы, так же по понятным причинам, узнав, что клинические микробиологические лаборатории не предлагают тестирование антибактериальных комбинаций по своему усмотрению.
Есть несколько важных причин, по которым лаборатория не может просто протестировать ту или иную комбинацию препаратов по запросу. Во-первых, методы "шахматной доски" и "тайм-килл" - это трудоемкие методы, для выполнения которых у большинства клинических лабораторий нет ресурсов или персонала, и, как обсуждалось выше, существуют некоторые ограничения в воспроизводимости. Однако помимо этих практических ограничений существует проблема интерпретации и клинической значимости синергетических тестов in vitro. В исследованиях синергизма противомикробных препаратов почти всегда изучаются либо тесты in vitro, либо клинические данные (которые обычно являются ретроспективными), но почти никогда эти два метода не используются в тандеме. В результате у нас мало понимания того, как результаты in vitro могут предсказать клинический ответ или какие методы или типы результатов в наибольшей степени отражают активность in vivo.
Еще в 2005 году было опубликовано рандомизированное двойное слепое исследование, в котором оценивались результаты у пациентов с муковисцидозом (МВ), получавших комбинированные схемы приема антибиотиков при легочных обострениях, которые были подобраны либо на основе обычного тестирования на чувствительность, либо на основе результатов комбинированного тестирования бактерицидных антибиотиков. Исследование не выявило улучшения исходов у пациентов, лечившихся по схемам, подобранным на основании результатов комбинированного тестирования. Поскольку это было одно из очень редких рандомизированных контролируемых клинических исследований в области синергетического тестирования, данная работа привлекла большое внимание и способствовала скептическому отношению к полезности синергетического тестирования при принятии клинических решений о лечении. Однако существуют ограничения даже для традиционного проведения AST для изолятов от людей с МВ, потому что условия жидкой культуры, которые составляют основу in vitro AST, сильно отличаются от биопленок, в которых такие патогены, как Pseudomonas aeruginosa, растут в легких пациентов с МВ. Поэтому неясно, насколько результаты этого исследования предсказывают полезность тестирования синергизма для других состояний, кроме легочных обострений МВ.
Очевидно, что нам необходимо больше данных, чтобы понять, какие методы тестирования синергизма предсказывают эффективность комбинированных препаратов в клинической практике, а также для стандартизации и упрощения этих методов. Методы, учитывающие поведение как препаратов, так и бактерий in vivo - методы, моделирующие фармакокинетические и фармакодинамические параметры - могут оказаться более полезными, чем "статичные" шахматные доски или исследования " тайм-килл", но они также более трудоемки.
Любой метод, который может быть принят для клинической лаборатории, также должен пройти тщательную оценку на точность и воспроизводимость, что является сложной задачей, поскольку параметры контроля качества для большинства методов синергетического тестирования четко не определены, и не существует установленного процесса одобрения синергетического тестирования регулирующими органами. В условиях, когда разработка антибиотиков не успевает за ростом множественной лекарственной резистентности, использование существующих противомикробных препаратов в комбинированных схемах может значительно расширить возможности лечения, и исследования по созданию и проверке практических, прогностических методов тестирования комбинированных антибиотиков будут иметь решающее значение.