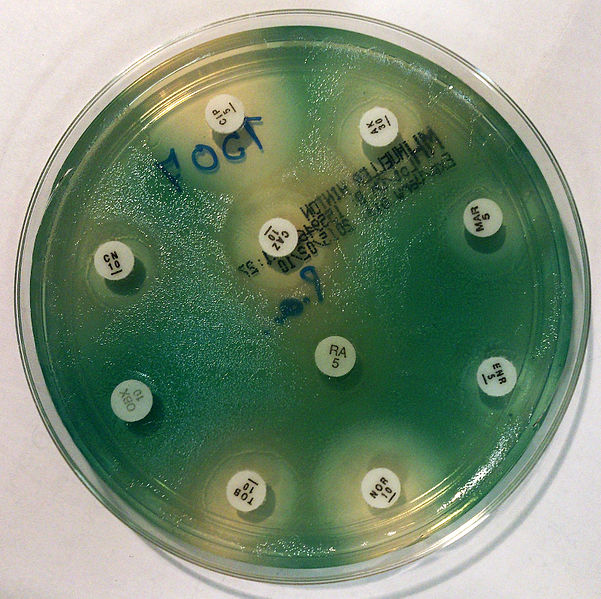
Антимикробные препараты могут оказывать специфические физиологические эффекты при их комбинированном применении, которые отличаются от тех, которые проявляются при их одиночном применении.
В то время как комбинированные эффекты были подробно изучены для комбинаций антибиотик-антибиотик, комбинированные эффекты антибиотиков с антимикробными препаратами, используемыми в качестве биоцидов или антисептиков, систематически не исследовались. В данном исследовании мы изучили влияние комбинаций антибиотиков (меропенем, гентамицин и ципрофлоксацин) и веществ, используемых в качестве биоцидов или антисептиков [октенидин, бензалкония хлорид, цетримония бромид, хлоргексидин, повидон-йод, нитрат серебра (AgNO3) и Ag-наночастицы] на скорость планктонного роста Pseudomonas aeruginosa.
Предполагается, что комбинированное воздействие нескольких антибиотиков улучшает результаты лечения, особенно при инфекциях, вызванных бактериями с множественной лекарственной резистентностью. Однако, в зависимости от условий, комбинированное лечение может ускорить или задержать селекцию резистентности. Поэтому выбор оптимальной комбинации требует знаний о возможных физиологических взаимодействиях между эффектами комбинированных активных веществ; то есть, являются ли их индивидуальные эффекты просто дополнительными, потенцированными (синергия) или буферизованными (антагонизм и супрессия) при использовании в комбинации (Baym et al., 2015).
Комбинаторные эффекты между антибиотиками, антимикробными пептидами и антибиотиками с факторами вирулентности были подробно изучены. Напротив, комбинаторным эффектам соединений, используемых в качестве дезинфицирующих средств, консервантов, антисептиков и антимикробных поверхностных покрытий (для простоты отныне называемых биоцидами) с антибиотиками уделялось меньше внимания (Brochado et al., 2018). Однако существует несколько ситуаций, в которых антибиотики и биоциды могут оказывать комбинированное воздействие на микроорганизмы.
Эти ситуации связаны с клиническими схемами лечения, в которых местное лечение микробных инфекций антисептиками подкрепляется системным дозированием антибиотиков; например, лечение хронических ран и имплантация медицинских устройств, покрытых антимикробными препаратами. Кроме того, микробы могут подвергаться воздействию комбинаций антибиотиков и биоцидов в определенных средах, таких как сточные воды больниц или очистных сооружений.
В данной работе мы исследуем комбинаторное воздействие антибиотиков и биоцидов на патоген Pseudomonas aeruginosa. Мы выбрали P. aeruginosa, поскольку этот патоген широко распространен в клинических ситуациях, в которых встречаются антибиотики и антисептики или биоциды; например, он часто встречается при раневых инфекциях, известно, что он колонизирует медицинские имплантаты и известно, что он широко распространен в окружающей среде. Мы выбрали три антибиотика, которые используются для лечения инфекций P. aeruginosa, и семь биоцидов, охватывающих различные классы, способы действия и области применения.
Эффекты комбинаций были исследованы в ростовых экспериментах в микротитровальных планшетах при различных концентрациях, и были рассчитаны баллы взаимодействия Блисса. Биоциды со схожим химическим составом в большинстве случаев демонстрировали последовательное взаимодействие с различными антибиотиками. Например, катионные поверхностно-активные вещества (октенидин) и катионные четвертичные аммониевые соединения [QACs, например, бензалкония хлорид (BAC)] были антагонистичны с меропенемом и синергичны с гентамицином. Однако CTAB, который также является катионным QAC, не показал взаимодействия с меропенемом и был антагонистом гентамицина. Более того, AgNO3 и наночастицы серебра (AgNP) были антагонистичны с меропенемом и синергичны с гентамицином.
Наблюдаемые взаимодействия между антибиотиками и серебром согласуются с предыдущими сообщениями, в которых был показан синергетический эффект между аминогликозидами и серебром на уничтожение планктонной Escherichia coli (Morones-Ramirez et al., 2013) и биопленок P. aeruginosa (Habash et al., 2017), а также отсутствие эффекта на планктонный рост P. aeruginosa ATCC 10145 для комбинации ципрофлоксацин-AgNP (Markowska et al., 2014). В отличие от этого, антагонистический эффект между AgNP и меропенемом, очевидный в наших данных, ранее не наблюдался у P. aeruginosa ATCC 10145 (Markowska et al., 2014). Кроме того, ранее был описан штаммоспецифический синергический эффект между хлоргексидином и гентамицином для клинических изолятов P. aeruginosa (Barnham and Kerby, 1980), в то время как наши данные показывают антагонистический эффект для штамма MPAO1.
В данном исследовании мы представляем первый комплексный анализ физиологических взаимодействий комбинаций антибиотиков и биоцидов у P. aeruginosa. Эти данные послужат основой для разработки улучшенных протоколов лечения, в которых биоциды/антисептики и антибиотики используются в комбинации. Это может быть особенно важно в ситуациях, когда эти антимикробные препараты создают градиенты концентрации. Такие градиенты могут привести к установлению соответствующих комбинаторных концентраций, которые затем могут привести к комбинированному воздействию на рост.
Полученные результаты создают основу для дальнейшей работы, которая должна быть направлена на:
(i) подтверждение эффектов комбинации с другими установленными концепциями, такими как аддитивность Loewe (включая факториальную ингибирующую концентрацию; Hallander et al., 1982),
(ii) расширение проверки эффектов комбинации с другими антибиотиками,
(iii) картирование возникновения комбинированных эффектов у клинических изолятов P. aeruginosa и других патогенов, и
(iv) изучение молекулярного механизма, лежащего в основе комбинированных эффектов, с помощью исследований экспрессии генов или нокаутов.
Более того, будущие исследования должны изучить потенциальные эволюционные последствия эффектов физиологического взаимодействия между антибиотиками и биоцидами. Это актуально, поскольку было показано, что характер физиологического взаимодействия (синергия или антагонизм) лежит в основе селекции за или против резистентных к антимикробным препаратам штаммов в конкуренции с чувствительными штаммами, подвергающимися воздействию комбинаций антимикробных препаратов.