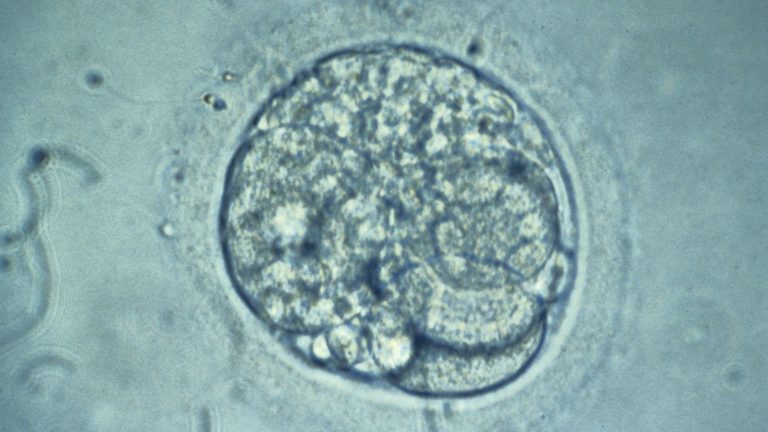
Когда в 2016 году родился первый ребенок, зачатый с помощью метода, в котором использовался генетический материал трех человек, ученые обеспокоились тем, что эта процедура не была достаточно изучена, чтобы убедиться в ее безопасности.
Недавно ученые из Китая провели первое комплексное исследование этой методики на эмбрионах человека на ранней стадии развития и сообщают, что она, похоже, не влияет на их развитие. Техника использования генетического материала трех человек для создания эмбрионов разработана для того, чтобы матери с дефектами митохондрий - органелл, обеспечивающих клетки энергией, - не передали их своим детям. Митохондрии содержат собственную ДНК, и дети наследуют все свои митохондрии от матери.
"Заместительная митохондриальная терапия - спорная область", - говорит соавтор исследования Вэй Шанг, акушер-гинеколог из Главного госпиталя китайской армии НОАК в Пекине. "Своим исследованием мы надеемся заложить основу для развития этой методики".
Шанг и ее коллеги изучали безопасность одного из трех основных видов заместительной митохондриальной терапии, называемой "переносом веретена", который был использован для создания первого ребенка с генетическим материалом от трех человек, родившегося в Мексике в 2016 году. В этом методе ядерная ДНК из яйцеклетки женщины с дефектными митохондриями переносится в донорскую яйцеклетку со здоровыми митохондриями, у которой была удалена ядерная ДНК. Затем яйцеклетка оплодотворяется спермой отца in vitro. Получившийся эмбрион содержит гены обоих родителей в дополнение к митохондриальным генам донора.
В рамках исследования команда сравнила десятки человеческих эмбрионов, прошедших процедуру переноса веретена, с контрольной группой эмбрионов. Обе группы эмбрионов развивались в течение одной недели после оплодотворения. Исследователи обнаружили, что клетки пятидневной "бластоцисты" в обеих группах имели почти одинаковый уровень экспрессии и транскрипции генов, что говорит о том, что перенос веретена не влияет на раннее эмбриональное развитие. Авторы сообщили о своих результатах в журнале PLoS Biology в прошлом месяце.
"Это первое [исследование], в котором было проведено такое всестороннее сравнение человеческих эмбрионов, созданных с помощью переноса веретена", - говорит Дитрих Эгли, биолог стволовых клеток из Колумбийского университета в Нью-Йорке. Он добавляет, что работа является "уникальной и потрясающей" благодаря своему высокому качеству и количеству данных, которые она предоставляет. Эгли говорит, что безопасность переноса веретена была ожидаема - благодаря данным предыдущих исследований на животных и здоровому ребенку, родившемуся в 2016 году, - но до сих пор не была окончательно доказана.
Примерно один из 5 000 детей рождается с заболеваниями, вызванными вредными мутациями в их митохондриальной ДНК. Дефектные гены могут привести к проблемам во многих органах, включая сердце и мозг. Пока что заместительная митохондриальная терапия кажется наиболее эффективным способом блокировать передачу этих генов потомству, объясняет Эгли.
Но Мин Цзян, специалист по митохондриальной биологии из Университета Вестлейк в Ханчжоу, Китай, говорит, что долгосрочные последствия заместительной митохондриальной терапии остаются неясными. При использовании существующих методов небольшое количество митохондриальной ДНК матери непреднамеренно переносится в донорскую яйцеклетку, обычно составляя менее 2% от общего количества митохондрий эмбриона. Шанг утверждает, что они усовершенствовали методику, чтобы сделать этот уровень "почти необнаружимым", но Цзян предупреждает, что, согласно исследованиям, доля материнской митохондриальной ДНК может увеличиваться по мере развития клеток , повышая риск развития митохондриальных заболеваний у потомства.
"Материнские митохондрии и ядро сосуществуют долгое время, поэтому, возможно, ядро может предпочитать клетки с материнскими митохондриями", - отмечает Цзян, добавляя, что взаимодействие между этими двумя органеллами требует дополнительных исследований. "Пока что исследования показывают, что перенос веретена работает. Но долгосрочное здоровье детей, родившихся с помощью этой терапии, необходимо изучить в ходе клинических испытаний", - говорит она.
Только несколько стран, включая Великобританию и Австралию, одобрили терапию замещения митохондрий. Эта методика запрещена в США; в Китае ее использование в качестве лечения бесплодия было запрещено в 2003 году, но правительство не уточнило, запрещен ли этот метод как способ предотвращения наследования детьми митохондриальных заболеваний.
Шанг рассказывает, что группа планировала провести клинические испытания заместительной митохондриальной терапии в Китае. Китайское законодательство не содержит прямого запрета на такие испытания. Но после скандала с "ребенком CRISPR" команда сместила акцент на сбор большего количества данных о безопасности лабораторных исследований. В 2018 году китайский ученый Хэ Цзянькуй потряс мир, объявив, что использовал метод редактирования генов CRISPR-Cas9 для генетического редактирования ДНК эмбрионов, впоследствии имплантированных женщине. Международные ученые широко осудили использование им CRISPR в эмбрионах как рискованное и неэтичное, и он был заключен в тюрьму за ведение незаконной медицинской практики.
Эгли говорит, что исследование безопасности пересадки веретена предоставит важные данные, которые помогут регулирующим органам в странах, где эта процедура не разрешена, оценить ее безопасность и эффективность. "Это действительно может помочь продвинуться в данной области", - говорит он.