Если ничего не менять, то к 2050 году ожидается, что ежегодно 10 миллионов человек будут умирать от заболеваний, резистентных к лекарственным препаратам.
Посыл ясен: необходимо найти альтернативные методы лечения или столкнуться с реальностью, в которой когда-то излечимые инфекции становятся причиной смерти, которую можно было предотвратить.
Фаговая терапия предполагает использование фагов для лечения бактериальных инфекций. Фаги встречаются повсюду - от почвы до нашего кишечника, их существует тысячи различных видов. В отличие от многих антибиотиков, которые уничтожают вредные бактерии, одновременно разрушая микробиоту (что приводит к возникновению новых проблем), каждый фаг эволюционировал для более узкой направленности на штаммы или виды бактерий. Такая специфичность делает фаговую терапию привлекательной альтернативой для лечения инфекций, особенно вызванных бактериями с множественной лекарственной резистентностью (MDR).
Тем не менее, фаговая терапия в основном существует на задворках медицины, особенно в западных странах, таких как США, где она иногда одобряется для сострадательного применения (т.е. используется в чрезвычайных обстоятельствах, когда другие разрешенные методы лечения недоступны). Почему? И что должно произойти, чтобы фаговая терапия стала общепринятой? Ответы на эти вопросы кроются в скептическом отношении к истории, нормативным и производственным препятствиям и физиологическим особенностям самих фагов.
Взлет и падение фаговой терапии на Западе
Фаговая терапия не является чем-то новым - ее истоки берут начало более 100 лет назад. Французско-канадскому микробиологу Феликсу д'Эрелле приписывают открытие и присвоение имени бактериофагам (хотя ведутся споры о том, кто был официальным первооткрывателем фага - д'Эрелле или британский микробиолог Фредерик Творт). В любом случае, использование д'Эрелле фагов для борьбы с бактериальными инфекциями дало толчок международным усилиям, в основном сосредоточенным в бывшем Советском Союзе, по проверке эффективности фаговой терапии для лечения брюшного тифа и холеры.
Первые исследования были многообещающими, хотя эксперименты часто были неправильно спланированы по современным стандартам (например, в них отсутствовали плацебо или контрольные группы). Результаты публиковались в неанглоязычных журналах, что делало их практически недоступными для западных ученых. Тем не менее, фаговая терапия не обошла стороной и США. В 1940-х годах несколько американских фармацевтических компаний выпускали фаговые препараты для лечения различных инфекций, включая инфекции верхних дыхательных путей и абсцессы.
Однако фаговая терапия в конце концов вышла из практики на Западе по нескольким причинам. Во-первых, ученые скептически относились к тому, насколько хорошо она работает. Неправильное хранение или очистка фагов, вероятно, сыграли свою роль. Например, ранние коммерческие препараты включали "консерванты", такие как фенол, который денатурировал и инактивировал фаги. Ученые также не понимали, что фаги являются высокоспецифичными для бактерий, против которых они направлены - фаговые препараты часто использовались для лечения бактериальных инфекций, которые не были восприимчивы к терапевтическому фагу (фагам).
Социальные факторы также были важны. После Второй мировой войны исследования и применение фаговой терапии продолжились в странах Восточной Европы, где они продолжаются и по сей день. Действительно, фаговая терапия до сих пор является обычной медицинской практикой в Грузии, Польше и России. Однако война заставила ученых в Западной Европе и США избегать фаговой терапии, учитывая ее тесную связь с бывшим Советским Союзом. Открытие пенициллина стало последним гвоздем в крышку гроба фаговой терапии - появление антибиотиков произвело революцию в лечении бактериальных инфекций и стало золотым стандартом во многих странах мира.
Возрождение фаговой терапии
Однако за последнее десятилетие фаговая терапия пережила ренессанс в США, отчасти подстегиваемая растущей угрозой AMR. Стеффани Стратди, заместитель декана факультета глобальных наук о здоровье, соучредитель и содиректор Центра инновационного применения фагов и терапии (IPATH - первый специализированный центр фаговой терапии в Северной Америке) при Калифорнийском университете в Сан-Диего (UCSD), находится в авангарде развития фаговой терапии.
Приобщение Стратди к фаговой терапии обусловлено личным опытом. В 2015 году ее муж, доктор Том Паттерсон, профессор психиатрии в Медицинской школе UCSD, во время отпуска в Египте заразился смертельной инфекцией, вызванной MDR Acinetobacter baumannii. Никакие антибиотики не могли справиться с его инфекцией. Врачи в основном говорили: "Мы больше ничего не можем сделать"... И мы видели, как он угасал на наших глазах", - вспоминает Стратди.
Поскольку время поджимало, она прочесала Интернет в поисках чего-нибудь - чего угодно, - что могло бы спасти Паттерсона. Статья о фаговой терапии заинтересовала ее, и она предложила эту идею врачам Паттерсона, которые с одобрения Управления по контролю за продуктами и лекарствами США (FDA) согласились попробовать.
Для поиска фагов, способных убить штамм A. baumannii Паттерсона, команда прибегла к помощи исследователей из Центра фаговых технологий при Техасском университете A&M, а также ученых из ВМС США. Охота на фагов, которая включала в себя прочесывание уже существующих библиотек фагов (т.е. коллекций фагов, ранее выделенных из различных источников) и выделение новых фагов из сточных вод, отходов животноводства и даже трюмов кораблей ВМС, увенчалась успехом. После внутривенного введения фагового коктейля Паттерсону почти сразу стало лучше. Он полностью выздоровел и через 9 месяцев после поступления в больницу вернулся домой. Четыре года спустя Паттерсон и Стратди опубликовали книгу "Идеальный хищник", в которой описали эту историю.
Благодаря громкому делу Паттерсона исследования фаговой терапии оказались в центре внимания. За последние несколько лет в США и странах Западной Европы появляется все больше тематических исследований, подчеркивающих эффективность фаговой терапии для лечения различных MDR-инфекций, от легочных инфекций у больных муковисцидозом до инфекций мочевыводящих путей.
Проблемы развития фаговой терапии
Тем не менее, хотя фаговая терапия больше не находится на задворках медицины в США, она не находится и на переднем крае. "Одна из главных причин, почему фаговая терапия сейчас не является основной на Западе, заключается в том, что клинические испытания не показали ее эффективность", - объясняет Стратди. Она отметила, что клинические испытания составляют основу разработки терапевтических препаратов в США - неофициальных доказательств и/или изучения конкретных случаев недостаточно.
Существует 2 типа фагов: литические и умеренные. Строго литические фаги инфицируют клетку-хозяина и вызывают ее разрушение, тем самым убивая бактерию. Умеренные, или лизогенные, фаги не убивают свою бактериальную жертву сразу - они интегрируют свой геном (который может содержать гены AMR или токсинов) в клетку хозяина. В конечном итоге фаг может лизировать клетку, но это мало что дает для немедленного предотвращения бактериальной инфекции и может способствовать распространению AMR и других генов вирулентности. Поэтому очень важно, чтобы для фаговой терапии использовались строго литические фаги.
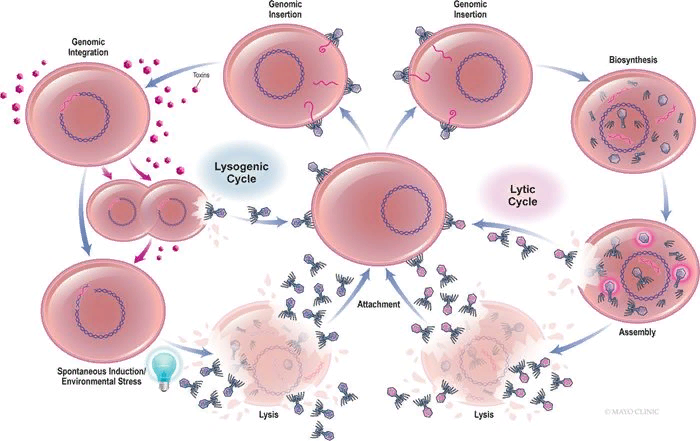
Литические фаги реплицируются внутри бактерий и лизируют клетку-хозяина сразу после сборки. В лизогенном цикле фаги интегрируют свой геном в геном клетки-хозяина.
Учитывая это, процесс выявления фагов для лечения инфекции может быть длительным. Он часто включает в себя тестирование фагов из существующих библиотек, чтобы найти те, которые убивают бактериальный изолят пациента. "Это все равно что [иметь] миллион ключей и пытаться разобраться в миллионе замков, чтобы понять, какой ключ подходит к замку", - объясняет Стратди. В одном из исследований сообщалось, что с момента запроса на фаговую терапию до фактического введения препарата пациенту проходит от 28 до 386 дней.
Однако в настоящее время разрабатываются препараты с более широким целевым диапазоном. Например, компания Locus Biosciences, занимающаяся разработкой фаговых биотерапевтических препаратов, производит фаговые коктейли для каждого из 4 различных патогенов (Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa и Staphyloccocus aureaus), которые действуют на >95% клинических штаммов. Этот подход не требует культивирования изолята пациента и скрининга библиотеки нужных фагов, что может упростить процесс.
В отличие от антибиотиков, концентрация препарата в организме которых со временем снижается, фаги размножаются. Это означает, что доза фагового коктейля, которую вводят пациенту, не обязательно является той дозой, которую он получает. Как эта самовоспроизводящаяся особенность фаговых терапий влияет на эффективность лечения и возможность побочных эффектов, пока неизвестно. "[Нам нужны] фармакокинетические и фармакодинамические исследования, чтобы попытаться выяснить: окей, [если] вы доставите это количество фага, но этим конкретным путем, что дальше произойдет с фагом?"", - комментирует Стратди.
Аналогичным образом, исследователи должны подтвердить, "что [фаги] работают в той среде, в которой они должны работать", - говорит Ник Конли, вице-президент по технологиям компании Locus Biosciences. Например, если фаги используются для лечения инфекции мочевыводящих путей (ИМП), они должны быть активны в моче.
Существуют также важные аспекты с точки зрения производства. Например, для создания фаговых препаратов фаги усиливаются в бактериях-хозяевах - они заражают бактерии, бактерии лизируются и выделяют больше фагов для создания высококонцентрированного фагового бульона. Однако при лизисе "все внутренности бактерий выливаются наружу", - объясняет Конли. Это включает токсины и ДНК, а также другие компоненты клеток, которые должны быть удалены, прежде чем фаг можно будет, например, ввести в кровь человека.
Пациенты обычно получают смеси (коктейли) фагов, которые по-разному воздействуют на бактерии. Вероятность развития резистентности бактерий к нескольким фагам ниже, чем к одному фагу - ниже, но не исключается. Пациенты, получающие фаговую терапию, должны находиться под постоянным наблюдением, чтобы убедиться, что фаги по-прежнему эффективны против их инфекции. Если нет, исследователи должны найти новый набор фагов, способных бороться с патогеном.
Тем не менее, развитие резистентности не всегда плохо. В некоторых случаях модификации бактерий, способствующие развитию резистентности к фагам, повышают их восприимчивость к антибиотикам и, таким образом, работают синергетически с антибиотиками, повышая их эффективность.
Будущее фаговой терапии
Несмотря на трудности, перспективы фаговой терапии многообещающие. Стратди подчеркнула, что FDA "в курсе" фаговой терапии и, по словам Конли, "очень вдумчиво и разумно" подходит к регулированию фаговых терапий. Национальные институты здравоохранения США (NIH) недавно выделили 2,5 миллиона долларов 12 институтам по всему миру на изучение фаговой терапии. Также проводятся клинические испытания, включая многоцентровое исследование фазы 1b/2, оценивающее микробиологическую активность одной дозы фаговой терапии у пациентов с муковисцидозом, хронически колонизированных P. aeruginosa. Кроме того, в июле 2022 года компания Locus начала исследование фазы 2/3, оценивающее безопасность, переносимость, фармакокинетику и эффективность фагового препарата для лечения острых неосложненных ИМП, вызванных MDR E. coli.
Ученые также изучают возможность оптимизации фаговых препаратов для создания более эффективных методов лечения. Компания Locus, например, разрабатывает фаговые терапевтические препараты, в которых используется технология CRISPR-Cas3. Фаги доставляют CRISPR-Cas3 своему бактериальному хозяину, который необратимо разрушает бактериальную ДНК. По сравнению с обычными фагами это обеспечивает более надежное уничтожение. Конли подчеркивает, что способность модифицировать фаги, в том числе с помощью многих других не-Cas полезных нагрузок, укрепляет их потенциал в качестве ключевого инструмента для борьбы с AMR в будущем.
По мнению Стратди, будущее фаговой терапии находится в руках следующего поколения ученых. Существует растущее сообщество молодых исследователей, "которые действительно взволнованы перспективами фаговой терапии". Именно это рвение в сочетании с сотрудничеством, увеличением финансирования и продвижением клинических испытаний станет ключом к тому, чтобы вывести фаговую терапию из тени. "Где есть желание, там есть и возможность".