Большинство материалов, используемых нами в строительстве, производятся из химических веществ, получаемых из нефти (нефтехимии), которая является ограниченным ресурсом.
Одна из стратегий решения проблем, связанных с истощением этого ресурса, заключается в отказе от нефтехимии и переходе на возобновляемые ресурсы и химические вещества, производимые живыми организмами. Эта концепция получила название «биоэкономика». Возникающий международный интерес к биоэкономике способствует развитию исследований, направленных на получение конкретных ответов на вопросы устойчивого развития, и микроорганизмы обладают многими метаболическими инструментами, необходимыми для успешной реализации этой идеи.
С идеей биоэкономики тесно связана концепция возобновляемости или цикличности. Цикличные продукты и материалы действительно можно перерабатывать, а не разлагать, как при химической (традиционной) переработке. И снова микробы уникально подходят для осуществления метаболических процессов, которые расщепляют сложные продукты и восстанавливают их в пригодные для использования ресурсы. Однако многие микроорганизмы, которые могут стать движущей силой биоэкономики, не обладают генетическим инструментарием, который позволил бы их индустриализировать, и исследователи используют достижения в области микробной инженерии для решения этих проблем.
Часто полный метаболический путь, необходимый для осуществления цикличности, не встречается в природе. Напротив, различные этапы расщепления и переработки сложных материалов могут происходить в нескольких организмах. Такое распределение функций между несколькими микроорганизмами может быть неудобным в промышленных условиях, так как каждый организм будет иметь индивидуальные требования к росту, которые должны быть удовлетворены, что усложняет процесс. Один из подходов к решению проблемы сложности поддержания микробных сообществ заключается в объединении всех необходимых генов в одном организме для биопроизводства. Этот подход называется консолидированным биопроцессингом (КБП). Цель КБП - оптимизировать работу сложного сообщества, объединив все процессы распада и восстановления интересующих химических веществ в одном организме.
КБП может применяться во многих контекстах. Например, для использования биологических процессов для производства авиационного топлива из растительной биомассы потребуются организмы КПБ. Эти организмы будут расщеплять сложную растительную биомассу и химически преобразовывать ее в желаемый конечный продукт. Цель внедрения КБП - упростить процесс и снизить затраты, чтобы сделать промышленное производство реалистичным.
Однако для создания микроорганизма с КБП может потребоваться сложная генная инженерия, если в природе не существует ни одного организма, который содержал бы все необходимые гены для расщепления данного материала и превращения его в полезный ресурс. Генная инженерия включает в себя ряд методов, которые используются для изменения существующих генов организма с целью получения определенных фенотипов, включая выполнение интересующей функции. Часто целью является добавление новых генов, которые придают целевому организму желаемую функцию и организм, выбранный в качестве отправной точки для инженерии, называют организмом-шасси. Но как исследователи и промышленные микробиологи выбирают идеальный организм-шасси для своих задач?
Можно было бы склониться к выбору модельного организма, такого как Escherichia coli или Bacillus subtilis, для которых уже существуют хорошо отлаженные генетические протоколы, но оказывается, что уникальные инженерные вопросы требуют уникальных стратегий, которые часто направляют внимание ученых на менее знакомые микроорганизмы. Происходит ли интересующий нас процесс в сложных условиях, например при высоких температурах, или образуются побочные продукты, токсичные для некоторых организмов? В этих случаях ученым важно выбрать теплолюбивый организм или организм, устойчивый к токсичным побочным продуктам, соответственно. Однако очень немногие из этих признаков присутствуют у модельных организмов, поэтому проще разработать инструменты для генетического манипулирования немодельными организмами.
Стратегии генной инженерии
Поглощение ДНК: электропорация, конъюгация и нативная компетентность
Работа с немодельными организмами, такими как Clostridium thermocellum и Parageobacillus thermoglucosidasius, может создать значительные препятствия для генной инженерии. Во-первых, ученые должны побудить интересующий их микроб «принять» или включить чужеродный генетический материал в свой геном. Типичные методы, которые ученые используют, чтобы побудить организмы в лаборатории принять ДНК, которая не является родной для их собственных геномов, включают электропорацию, конъюгацию и нативную компетентность.
Электропорация: этот метод использует электрический разряд для создания временных пор в клеточной оболочке, которые затем позволяют ДНК проникнуть в клетку. Электропорация - широко используемый метод и инноваций в этой области не так много. Однако совершенствование подходов с высокой пропускной способностью, например роботов для обработки жидкостей, позволяет увеличить скорость отбора различных условий (например, различных электропорационных сред и напряжений для электропорации), которые могут обеспечить поглощение ДНК.
Конъюгация: этот метод использует бактерию-донора для передачи ДНК интересующей бактерии через пилус при контакте.
Нативная компетентность: этот метод основан на фенотипе, которым обладают некоторые организмы (так называемая нативная компетентность), что позволяет клеткам поглощать ДНК из окружающей среды и включать ее в свой геном. Важно отметить, что не все виды обладают этой способностью, а условия, вызывающие компетентность, зависят от штамма.
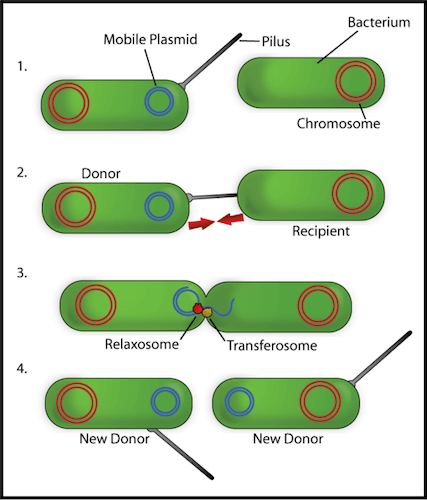
Бактериальная конъюгация - полезная техника переноса ДНК от бактерии-донора к бактерии-реципиенту при непосредственном контакте через пилус. Источник: Wikimedia Commons.
Сохранение ДНК: системы рестрикционной модификации и выбор маркеров
После того как ДНК попала в клетку, важно уметь ее сохранить. Другими словами, целевая ДНК должна реплицироваться, транскрибироваться и транслироваться как часть нормальных биологических процессов организма. Поддержание ДНК и последующая экспрессия генов в бактериальном хозяине могут быть затруднены защитными системами бактерий. Например, системы рестрикционной модификации позволяют бактериям идентифицировать «собственную» ДНК, сканируя внутриклеточную ДНК ферментами рестрикции на наличие специфических схем метилирования, а затем разрушая ДНК, которая не метилирована должным образом. Схема метилирования в геноме микроорганизма называется метиломом. Большинство ДНК, которые ученые пытаются трансформировать в интересующие их бактерии, либо не метилированы, либо метилированы в соответствии с шаблоном метилирования клонированного штамма E. coli. Таким образом, если ДНК, которую пытаются внедрить ученые, окажется несамостоятельной, системы рестрикционной модификации впоследствии разрушат ее.
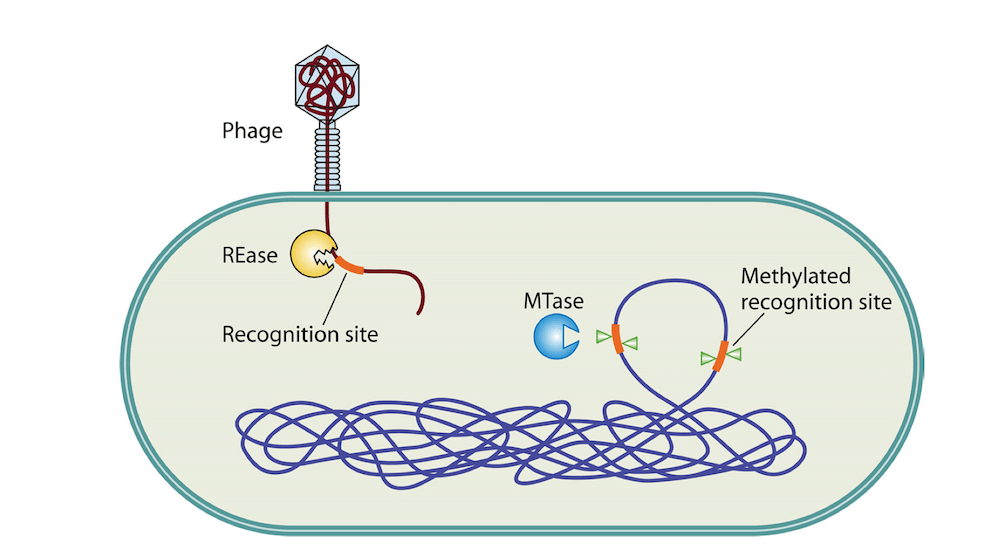
Системы рестрикционной модификации (R-M) распознают статус метилирования входящей чужеродной ДНК. Метилированные последовательности распознаются как собственные, а последовательности на входящей ДНК, не содержащие метилирования, распознаются как несамостоятельные и расщепляются эндонуклеазой рестрикции (REase). Источник: Vasu K. et al./MMBR, март 2013 г.
Характеристика систем рестрикционных модификаций организма-реципиента - метод, который становится все более популярным, помогая обойти естественные защитные механизмы бактерий и побудить интересующий микроб принять новую ДНК в свой геном. Для этого проводится секвенирование метилома микроба с помощью таких методов, как нанопоровое секвенирование или секвенирование HIFI. После вычислительной идентификации паттернов метилирования исследователи могут определить белки, которые производят этот паттерн метилирования, - метилазы. После определения метилазы ее можно гетерологично экспрессировать в штамме E. coli, который будет метилировать ДНК, например плазмиду, в соответствии с паттерном метилирования интересующего организма, чтобы снизить вероятность ее деградации после трансформации. Эта способность имитировать паттерны метилирования быстро увеличивает вероятность и частоту генетической инженерии новых организмов-шасси.
Еще одним препятствием для сохранения ДНК и долгосрочного использования организма является отбор маркеров. Во многих стратегиях редактирования генома используется селективный маркер, например ген резистентности к антибиотикам, для селективного выращивания организмов, подвергшихся редактированию. В промышленных масштабах стоимость среды для выращивания имеет еще большее значение, чем в стандартных лабораторных экспериментах. Поэтому полезно избегать систем экспрессии генов на основе плазмид, которые часто требуют добавления антибиотиков в ростовую среду для поддержания роста.
В отсутствие систем экспрессии на основе плазмид гены должны быть интегрированы в геном хозяина, что может быть сложной задачей, если организм не обладает высокоактивным механизмом гомологичной рекомбинации. Одна из методологий, которая была использована для решения этой проблемы, называется серин-интегразной геномной инженерией (SAGE). В этом процессе генетический груз (набор генов) с обеих сторон фланкируется специфической ДНК, которую распознает рекомбинационный белок и использует для интеграции в определенные последовательности ДНК в геноме. По сравнению с более привычными тирозиновыми рекомбиназами, такими как Flp и Cre, сериновые рекомбиназы используют 2 уникальных участка, а не сильно похожие участки, которые подвержены последующей рекомбинации и потенциальной нестабильности. Возможность использования SAGE во многих микроорганизмах делает эту технологию перспективным инструментом для немодельных микробных шасси.
Хотя в этой статье описаны лишь несколько генетических стратегий, позволяющих распространить генетические технологии на новые микроорганизмы, многие из подобных стратегий могут быть уже на горизонте. Расширение нашего генетического репертуара - важный шаг на пути к созданию будущего, основанного на микробиологическом производстве. Чтобы достичь этого, нам необходимо разработать высокоэффективные методы модификации генома любого организма.
Микробы давно стали нашими партнерами, и чем больше мы узнаем о них, тем больше мы сможем использовать их для выполнения полезных задач, например, заменить пластмассы и топливо на основе нефти биоразлагаемыми пластмассами и биотопливом.

