Международная группа ученых выявила новую связь между определенными молекулами, производимыми микробиомом, и функцией белка, влияющего на воспаление кишечника.
Это открытие приближает исследователей к пониманию того, как хороший баланс микроорганизмов в нашем кишечнике связан с иммунной системой организма и здоровьем кишечника. Это также повышает возможность поиска новых методов лечения изнурительных воспалительных заболеваний кишечника, таких как язвенный колит и болезнь Крона. Авторы исследования выделили два класса молекул: короткоцепочечные жирные кислоты и вторичные желчные кислоты. Обе молекулы существуют в кишечнике в полезных количествах только тогда, когда определенным микроорганизмам создаются правильные условия для процветания в микробиоме. Выводы исследователей подтверждают растущий объем доказательств того, что здоровье микробиома человека, а значит и его общее самочувствие, тесно связано с питанием.
Микробиом кишечника различается у разных людей, но в целом известно, что соответствующий баланс ключевых микробов способствует здоровью кишечника. Этот баланс может быть нарушен изменениями в рационе питания. В частности, "западная" диета с высоким содержанием простых сахаров и жиров и низким содержанием растительного белка связана с уменьшением количества бактерий в кишечнике, вырабатывающих короткоцепочечные жирные кислоты и вторичные желчные кислоты.
P-гликопротеин (P-gp)- белок, изучаемый в данной работе, играет важнейшую роль в защите кишечного эпителия, опосредуя эффлюкс лекарств/ксенобиотиков из слизистой оболочки кишечника в просвет кишечника. Недавние исследования показали, что P-gp также является критическим звеном в коммуникации между барьерной функцией слизистой оболочки кишечника и врожденной иммунной системой. Однако, несмотря на то, что уже более 10 лет известно, что P-gp играет центральную роль в гомеостазе желудочно-кишечного тракта, точный молекулярный механизм, контролирующий его функциональную экспрессию и регуляцию, остается неясным.
Высокий уровень этого белка коррелирует со здоровым кишечником, при воспалительных заболеваниях кишечника экспрессия P-gp снижается. Однако, несмотря на понимание роли P-gp, до сих пор механизмы, контролирующие его экспрессию и регуляцию, оставались неизвестными. Результаты нового исследования в сочетании с более ранней работой, объясняют, как микробиом может влиять на экспрессию P-gp. Это дает важное представление о ключевом аспекте микробиома и о том, как он регулирует здоровье кишечника. Воспалительные заболевания кишечника связаны с генетикой и условиями окружающей среды, которые включают (но не ограничиваются ими) диету, физические упражнения, образ жизни и применение антибиотиков. Язвенный колит, наиболее распространенная форма воспалительного заболевания кишечника во всем мире, является хроническим, изнурительным заболеванием и хотя существующие методы лечения могут уменьшить воспаление и симптомы, на сегодняшний день нет ничего, что могло бы вылечить основное заболевание.
В более ранних исследованиях было продемонстрировано, что P-gp высвобождает противовоспалительные соединения в кишечнике. Эти молекулы, известные как эндоканнабиноиды, химически схожи с каннабисом, но вырабатываются человеческим организмом и играют ключевую роль в сдерживании воспаления в кишечнике. Если уровень эндоканнабиноидов снижается или полностью отсутствует, воспаление может усилиться. Молекулы, выявленные в новом исследовании, побуждают P-gp высвобождать эти важные молекулы эндоканнабиноидов.
Исследование, основывается на предыдущих данных, которые продемонстрировали, как противовоспалительный механизм P-gp постоянно уравновешивается провоспалительным процессом. Эти противоположные процессы взаимодействуют для поддержания здоровья кишечника: в отсутствие инфекции противовоспалительный путь P-gp активен для подавления ненужного воспаления, а провоспалительный путь готов запустить иммунный ответ для защиты от кишечной инфекции. При воспалительных заболеваниях кишечника, этот баланс нарушается.
Полученные группой результаты открывают новые возможности для лечения воспалительных заболеваний кишечника. Потенциальные будущие методы лечения могут включать доставку определенных бактерий или бактериальных продуктов в кишечник человека или изменения в рационе питания, которые будут поддерживать микробиом для стимулирования или поддержания экспрессии P-gp в кишечнике, тем самым защищая от нежелательного воспаления.
Авторы сообщают: "Результат этого исследования заключается в том, что мы теперь знаем конкретные молекулы, производимые бактериями микробиома, которые связаны с P-gp и, следовательно, со здоровьем кишечника. Эти молекулы работают согласованно, стимулируя P-gp для увеличения высвобождения эндоканнабиноидных молекул, которые подавляют кишечное воспаление. Мы были рады обнаружить, что существует не только связь между микробиомом кишечника и регуляцией P-gp в кишечнике, но и то, что два класса микробных молекул действительно работают вместе, чтобы вызвать экспрессию P-gp".
Полученные данные свидетельствуют о том, что питание крупного микробного сообщества имеет решающее значение и может быть достигнуто с помощью процессов, влияющих на микробиом и производство метаболитов. Хотя пищевые волокна могут увеличить производство короткоцепочечных жирных кислот в толстой кишке, конкретные пищевые субстраты, необходимые для поддержания микробиома, способствующего экспрессии P-gp в толстой кишке, достаточной для ограничения гиперактивных иммунных реакций и поддержания гомеостаза, еще предстоит определить.
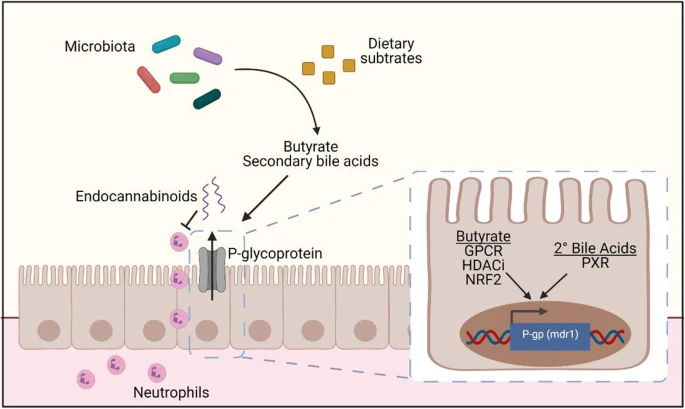
Рабочая модель экспрессии P-gp под влиянием микробиома.
Популяция бактерий, содержащая классы Bacilli и Clostridia, вызывает экспрессию P-gp в толстой кишке. Бутират и вторичные желчные кислоты, вырабатываемые этими бактериями из пищевых субстратов, вместе усиливают индукцию функциональной экспрессии P-gp на эпителии, который способен блокировать миграцию нейтрофилов путем эффлюкса своих эндогенных субстратов, эндоканнабиноидов.