Гематоэнцефалический барьер (ГЭБ) является важнейшей иммунологической особенностью центральной нервной системы (ЦНС) человека.
Состоящий из многих типов клеток, ГЭБ является структурным и функциональным барьером для микроорганизмов, таких как бактерии, грибы, вирусы или паразиты, которые могут циркулировать в кровотоке. Таким образом, ГЭБ является ключевым регулятором проникновения микроорганизмов в ЦНС и существует на границе кровеносных сосудов и интерстициальной жидкости мозга. ГЭБ также существует на других участках пересечения ЦНС и периферии, в том числе между кровью и клетками, вырабатывающими спинномозговую жидкость. Его задача - защищать и регулировать микросреду мозга. ГЭБ состоит из множества типов клеток. Эти клетки выстраиваются вдоль микрососудов мозга и работают согласованно, чтобы защитить ЦНС и ее нейроны от любых патогенов, находящихся на периферии.
ГЭБ - это сложная структура, следующая за лабиринтом сосудистой сети мозга. Он состоит из 4 типов клеток:
Эндотелиальные клетки. Эти клетки выстилают внутреннюю поверхность кровеносных сосудов. В ГЭБ они тесно связаны друг с другом через плотные соединения, образуя барьер. Эти клеточные соединения имеют решающее значение для микрососудов в нашем мозге, поскольку они поддерживают целостность и проницаемость сосуда, тем самым регулируя прохождение через BBB.
Перициты. Перициты, встроенные в базальную мембрану микрососудов, тесно связаны с эндотелиальными клетками ГЭБ. Считается, что перициты происходят от общего предшественника гладкомышечных клеток, и хотя они оказывают структурную поддержку микрососудам, они также взаимодействуют с эндотелиальными клетками, влияя на проницаемость и рост. В мозге перициты могут также выполнять функции, подобные иммунным клеткам, например, распознавать, поглощать и уничтожать потенциально опасные микроорганизмы, попадающие в кровь.
Астроциты. Астроциты, названные так за их звездообразную форму, являются опорными клетками, которые вносят свой вклад в структурные свойства ГЭБ. Известно, что астроциты привлекают периферические клетки, такие как лейкоциты, в ЦНС через ГЭБ.
Микроглия. Микроглия, являясь резидентными иммунными клетками ЦНС, располагается сразу за ГЭБ. Хотя их обычно не считают частью ГЭБ, микроглия обследует ЦНС на наличие микроорганизмов и обладает способностью поглощать и уничтожать обнаруженные микроорганизмы. Таким образом, микроглия является еще одной линией иммунологической защиты от потенциальных патогенов или токсинов, пересекающих ГЭБ.
ГЭБ эффективно защищает ЦНС, но, как и многие другие барьеры, он не совершенен. Остаются дискуссии о том, действительно ли ЦНС является иммунологически привилегированным местом, поскольку она не является непроницаемой для периферических клеток и микроорганизмов. Эта проницаемость вызывает вопросы. Как микроорганизмы проникают в ЦНС? Какие микроорганизмы могут пересекать ГЭБ?
Трансцеллюлярное проникновение в ЦНС
Микроорганизмы, которые пересекают ГЭБ трансцеллюлярным способом, попадают в ЦНС через эндотелиальные клетки. Они получают доступ к люминальной стороне эндотелия кровеносного сосуда, где проходят через сами эндотелиальные клетки. Преодолев барьер, эти микробы выходят через другую сторону клетки, которая находится в непосредственном контакте с астроцитами, микроглией и нейронами.
Существует 2 механизма трансцеллюлярного проникновения в ЦНС: абсорбционно-опосредованный и рецепторно-лигандный. Абсорбционно-опосредованный трансцитоз (АОТ) основан на взаимодействии зарядов вместо специфического связывания лиганда с рецептором. При AОТ неспецифическое взаимодействие с эндотелиальной мембраной приводит к поглощению белка, молекулы или микроба непосредственно в эндотелиальной клетке. Затем он транспортируется через клетку и высвобождается в ЦНС.
В отличие от этого, рецептор-лиганд-опосредованный трансцитоз (РЛТ) требует специфического связывания между микробом (лигандом) и эндотелиальной клеткой (рецептором). Хотя процессы поглощения для AОT и РЛТ схожи, взаимодействие хозяин-патоген требует гораздо большей специфичности, тем самым ограничивая способность микробов проникать в эндотелиальные клетки через РЛТ. К рецепторам, способствующим РЛТ, относятся рецептор трансферрина, рецептор инсулина и белки 1 и 2, связанные с рецептором липопротеина низкой плотности (LRP1 и 2).
Escherichia coli является популярной моделью для изучения переноса микроорганизмов через ГЭБ. Большинство штаммов кишечной палочки не опасны, однако отдельные штаммы кишечной палочки, такие как E. coli K1, обладают уникальной способностью уклоняться от иммунного ответа хозяина и достигать высокого уровня бактериемии, что может привести к развитию бактериального менингита. E. coli проникает в эндотелиальные клетки микрососудов головного мозга (ЭКГМ) в основном через РЛТ, используя несколько рецепторов, что приводит к связыванию E. coli и ЭКГМ хозяин-патоген. Эта патология наиболее часто встречается у новорожденных и может передаваться от матери к ребенку во время родов.
Парацеллюлярное проникновение в ЦНС
Микроорганизмы, пересекающие ГЭБ парацеллюлярным способом, проходят между эндотелиальными клетками, о чем говорит приставка "пара". Как при трансцеллюлярном, так и при парацеллюлярном проникновении в ЦНС микробы должны прикрепиться к ЭКГМ, прежде чем они будут перенесены. В этом сценарии микроорганизм прикрепляется к ЭКГМ и проникает в ЦНС между двумя эндотелиальными клетками. Во время этого механизма переноса микроорганизмов нарушается герметичное соединение, которое удерживает соседние эндотелиальные клетки вместе.
По сравнению с трансцитозом, меньшее количество микроорганизмов использует парацеллюлярный транспорт для проникновения в ЦНС. Treponema pallidum, бактерия, вызывающая сифилис, проникает в нервную систему на ранней стадии инфекции. Бактерия присутствует в межклеточных соединениях эндотелиальных клеток аорты, что позволяет предположить, что T. pallidum вторгается в ткани парацеллюлярно. Хотя лиганд микроба и рецептор эндотелиальных клеток, необходимые для первоначального связывания T. pallidum, неизвестны, T. pallidum, по-видимому, взаимодействует с тромбоцитами, влияя на проницаемость эндотелиальных клеток и способствуя проникновению через ГЭБ.
Инфицированные фагоциты (метод " троянского коня")
В отличие от прямого перемещения микроорганизма через ГЭБ при транс- и парацеллюлярном микробном переносе, метод "троянского коня" является непрямой формой микробного переноса. ГЭБ проницаем для фагоцитирующих лейкоцитов, которые регулярно циркулируют в крови для обеспечения иммунологического надзора, мигрируя в ткани и из них. Некоторые микроорганизмы кооптируют этот естественный процесс и используют его в своих интересах. В методе "троянский конь" перенос микроорганизмов происходит при миграции инфицированного фагоцита. Когда инфицированный лейкоцит пересекает ГЭБ, микроорганизм также получает доступ в ЦНС.
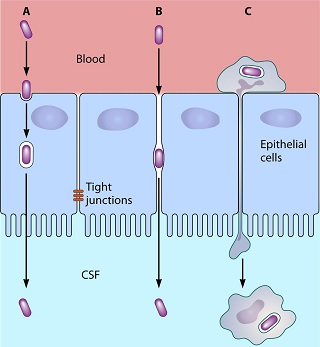
Три механизма переноса микроорганизмов через гематоэнцефалический барьер: A) трансцеллюлярный, B) парацеллюлярный и C) механизм инфицированного фагоцита (троянский конь).
Вирус иммунодефицита человека-1, ВИЧ-1, является лентивирусом, который проникает в ЦНС вскоре после системной инфекции. Хотя существует множество гипотез о том, как ВИЧ-1 попадает в ЦНС, передовой является гипотеза о том, что вирус попадает в ЦНС через механизм "троянского коня". Известно, что вирус инфицирует лейкоциты хозяина с помощью рецепторов CXCR4 и CCR5. Инфильтрирующие, инфицированные моноциты могут быть основным переносчиком ВИЧ-1 через ГЭБ.
Важно отметить, что эти способы переноса микроорганизмов не являются взаимоисключающими, и микроорганизмы могут использовать более одного пути для проникновения в ЦНС.
Менингит, сифилис и СПИД - три важные причины смерти во всем мире. Все три заболевания вызываются микроорганизмами, которые способны проникать в ЦНС и инфицировать ее, но, к сожалению, способность ГЭБ к защите также является препятствием для лечения.
Терапевтические подходы, разработанные в последнее десятилетие, используют существующие свойства и механизмы ГЭБ. Например, исследователи пытаются доставить нейрофармацевтические препараты в ЦНС с помощью векторов доставки, нацеленных на рецепторы на ЭКГМ, которые участвуют в РЛТ микробов. Нейрофармацевтические препараты также могут быть упакованы в биоразлагаемые наночастицы. Этот метод также использует существующие пути РЛТ для проникновения в ЦНС и может быть направлен на тканеспецифическое поглощение.
Нейротерапевтический дизайн включает в себя понимание нейроиммунологии ГЭБ и всего мозга. Лучшее понимание ГЭБ и механизмов проникновения микробов, наряду с новыми знаниями о сложной иммунной системе мозга, в конечном итоге поможет в разработке эффективных нейротерапевтических средств.