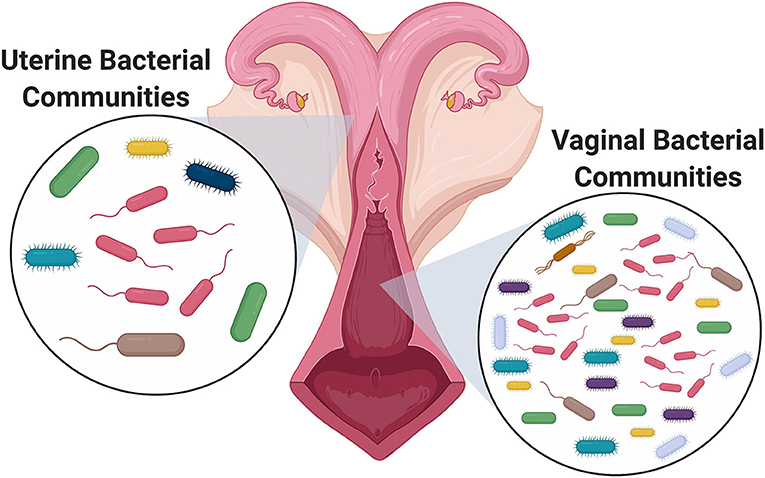
В недавнем исследовании, опубликованном в журнале Pathogens, ученые проанализировали текущее понимание состава и временной динамики микробных ниш в женском репродуктивном тракте.
Микробиота - это совокупность микробных популяций в определенной среде, в то время как микробиом представляет собой всю экосистему, включая геномы бактерий и хозяина, а также факторы окружающей среды. Эти факторы вносят свой вклад в результирующую функциональность/дисфункциональность экосистемы и влияют на метаболические пути, которые способствуют перекрестному взаимодействию между органами.
Было обнаружено, что некоторые заболевания, такие как диабет, ожирение, преждевременные роды, бактериальный вагиноз (БВ) и синдром раздраженного кишечника (СРК), связаны с изменением микробиоты. Растущий исследовательский интерес направлен на изучение связи метаболической активности кишечника с урогенитальным здоровьем. В данном исследовании ученые рассмотрели состав, временную динамику и характеристику микроорганизмов в женском репродуктивном тракте.
Здоровый микробиом влагалища описывается как микробиом, в составе которого преобладают представители семейства Lactobacillaceae. Они хорошо адаптированы и выступают в качестве первой линии защиты от колонизации патогенами. Побочный продукт ферментации, молочная кислота, помогает поддерживать низкий уровень pH влагалища между 3,5 и 4,2, подавляя многие вторгающиеся микробы. Кроме того, лактобациллы производят бактериоцины, которые действуют как антибиотики узкого спектра действия и защищают среду влагалища.
Исследователи определили пять различных типов состояния сообщества (CSTs I - V) микробиоты влагалища. В CST-I, -II, -III и -V преобладают лактобактерии, а в CST-IV присутствуют как облигатные, так и факультативные анаэробы. Из двух подтипов CST-IV дисбиотическим является только CST-IV-B. Женщины переходят от одной CST к другой во время менструального цикла. Различные исследования изучали CST для понимания динамики микробиома влагалища и показали, что здоровые женщины, скорее всего, поддерживают CST в течение двух-трех недель. В одном из исследований был сделан вывод, что частая смена CST и определенные виды бактерий в значительной степени предсказывают дисбиоз и симптоматические расстройства.
Более того, были зафиксированы межвидовые различия в микробном составе у представителей разных рас/этнических групп. Афроамериканки и испаноязычные женщины имеют преимущественно CST-IV-A, тогда как у женщин азиатского и кавказского происхождения преобладают Lactobacillus. CST также могут изменяться при циклических колебаниях эстрогена, рН, менструации, содержания гликогена, а также при привнесении экзогенных видов бактерий.
Эстроген повышает уровень Lactobacillus за счет увеличения доступности свободного гликогена в слизистой оболочке влагалища. Снижение уровня эстрогена и повышение уровня pH и железа из-за менструальной крови во влагалищном канале вызывают изменения микробного состава, что может повысить уязвимость к патогенам. Уровень эстрогена также снижается после менопаузы, а женщины в постменопаузе подвержены повышенному риску ИМП, БВ и других осложнений, связанных с дисбактериозом.
Сперма вызывает сложные изменения в микробиоме влагалища. Семенная жидкость содержит иммуноактивные молекулы, которые стимулируют/ингибируют воспалительные реакции женских половых органов и вызывают изменения в слизистой оболочке для ускорения изменений при беременности. В свою очередь, у женщин существует иммуносупрессивный механизм для предотвращения воспалительных реакций на сперму. Женщины выделяют окситоцин во время оргазма, что снижает вероятность воспалительной реакции на сперму.
Тем не менее, иммуносупрессия может сделать женщин восприимчивыми к неблагоприятному росту комменсалов и патогенных микробов, что может привести к инфекциям, передающимся половым путем. Кроме того, контрацепция также может влиять на микробную среду женщины. Гормональные внутриматочные контрацептивы вызывают изменения в уровне эстрогена, что приводит к защитным эффектам в микробиоме влагалища, в то время как оральные гормональные контрацептивы могут негативно влиять на связь между эстрогеном и кишечными бактериями.
БВ часто встречается у женщин репродуктивного и климактерического возраста и ассоциируется с неприятным запахом и выделениями. Он характеризуется снижением рН влагалища, потерей/уменьшением количества микробов, продуцирующих молочную кислоту, и повышением уровня факультативных и условно-патогенных анаэробов. В одном исследовании сообщалось об обратной связи между симптоматическим БВ и разнообразием уробиома. С БВ связаны серьезные последствия для репродуктивного здоровья, такие как сальпингит, аденомиоз, эндометрит и воспалительные заболевания органов малого таза. Более того, хронический/рецидивирующий БВ может повысить риск бесплодия и неблагоприятных исходов беременности. Первая линия терапии, рекомендуемая при БВ, - это метронидазол/клиндамицин. Однако было обнаружено, что после лечения метронидазолом БВ рецидивирует у 58% женщин, что указывает на необходимость совершенствования существующих терапевтических подходов к лечению БВ.
Патогенные бактерии/вирусы связываются с толл-подобным рецептором (TLR), вызывая реакцию хелперных Т-клеток первого типа (Th1) или Th17. Th1 ответ включает макрофаги, кластер дифференцировки 8 (CD8+) Т-клеток и интерферон (IFN)-γ, в то время как Th17 ответ характеризуется интерлейкинами (IL)-17A, IL-17F и IL-22. Патогенные бактерии заставляют нейтрофилы и макрофаги генерировать реактивные формы кислорода, которые влияют на окислительно-восстановительный потенциал и рН в матке и влагалище.
В одном из исследований было замечено, что у женщин с БВ окислительно-восстановительный потенциал и, следовательно, среда влагалища более снижены, чем у здоровых женщин. Короткоцепочечные жирные кислоты влияют на окислительно-восстановительный потенциал влагалища. Ухудшение среды может привести к иммунологическим изменениям и чрезмерному росту анаэробов, связанных с БВ, в экосистеме влагалища, что является причиной патогенеза БВ.
Определение эубиотического/здорового микробиома остается сложным. Хотя наблюдаются корреляции между состояниями болезни и конкретными видами бактерий, причины патогенеза болезни и факторы, влияющие на возвращение к гомеостазу, сложны. Хотя классификация по составу является ценной для распределения микробиома по категориям, имеются сообщения о том, что состав микроорганизмов индивидуален и иногда показывает корреляцию с состояниями заболевания. Авторы предложили изучить современные научные представления/гипотезы с помощью целостного экосистемного подхода, чтобы понять, что определяет здоровье в урогенитальном микробиоме.