Если больно мочиться, то это возможно... инфекция мочевыводящих путей (ИМП).
Это не такое уж редкое явление - ежегодно в мире происходит около 400 миллионов случаев ИМП, в основном у женщин. Хотя антибиотики вначале могут избавить от ИМП, инфекция часто возвращается снова и снова. Такие рецидивирующие ИМП - это в лучшем случае неприятность, а в худшем - почва для серьезных осложнений. Чтобы навсегда избавиться от этих инфекций, ученые пытаются выяснить, почему рецидивирующие инфекции вообще возникают.
Как правило, ИМП возникают, когда бактерии проникают в мочеиспускательный канал через уретру и попадают в мочевой пузырь. В 80% случаев виновником ИМП является уропатогенная Escherichia coli (UPEC), хотя их вызывают и другие бактерии (например, Proteus mirabilis и Klebsiella pneumoniae). Если кто-то перенес ИМП, вероятность того, что инфекция вернется, составляет 25-50%, а рецидивирующими ИМП считаются 3 и более инфекций в течение года. Чем можно объяснить этот удручающий круговорот?
Восприимчивость к рецидивирующим ИМП и ИМП в целом зависит от взаимодействия между хозяином и бактериями. Действительно, не у всех одинаковый риск заболеть ИМП, а сам термин «UPEC» охватывает целый ряд штаммов E. coli с незначительными различиями в их вирулентности и патогенезе. Для возникновения инфекции характеристики данного штамма E. coli должны точно совпадать с характеристиками данного хозяина, что описывается как своего рода механизм «замок и ключ».
Со стороны хозяина существует множество особенностей, которые способствуют росту и выживанию бактерий. Например, некоторые заболевания, такие как диабет, предрасполагают к развитию кишечных инфекций. У людей с диабетом, как правило, повышена концентрация глюкозы в моче. Бактерии UPEC потребляют эту глюкозу в качестве источника пищи, и, согласно исследованиям, их рост в моче, богатой глюкозой, более интенсивен, чем в обычной моче. Катетеры для дренажа мочевого пузыря - еще один ключевой игрок. Эти устройства создают основу для адгезии патогенов и образования биопленок, которые могут сохраняться даже после лечения антибиотиками, что приводит к рецидивам. Рецидивы ИМП также связаны с генетикой, неспособностью полностью опорожнить мочевой пузырь после мочеиспускания, что создает постоянный резервуар мочи для роста патогенов, частотой половой жизни и тщательностью гигиены после посещения туалета.
Почему последнее имеет значение? UPEC в основном обитают в кишечнике, где они могут существовать в качестве временного или комменсального члена микробиоты кишечника. После выведения с фекалиями бактерии поселяются на коже вблизи уретры или у женщин во влагалище. Из этих мест UPEC могут физически попасть в мочеиспускательный канал при подтирании (особенно при подтирании спереди назад), сексе или катетеризации.
В связи с этим возникают новые ассоциации между микробиотой кишечника и ИМП. Исследователи предполагают, что различия в микробном разнообразии кишечника и метаболической функции у женщин и имевших в анамнезе рецидивы ИМП, могут изменять иммунный ответ организма на бактериальную колонизацию мочевого пузыря через «ось кишечник-пузырь», предрасполагая к повторным инфекциям. Такое изменение иммунитета может быть связано и с самими ИМП. Недавно ученые обнаружили, что эпигеном стволовых клеток мочевого тракта, полученных от мышей с перенесенной или хронической инфекцией UPEC, различается. В частности, клетки хронически инфицированных мышей имели эпигенетические изменения в генах, которые регулируют связанные с ИМП изменения клеточной морфологии и воспаления. Полученные данные свидетельствуют о том, что ИМП вызывают длительные изменения в молекулярных процессах хозяина, повышающие восприимчивость к инфекции.
В конечном счете, возникнет ли у человека рецидивирующая инфекция или нет, зависит от биологических и поведенческих факторов, и риск может меняться в течение жизни. Конечно ИМП не существует без микробов, вызывающих инфекцию, и динамика развития таких микробов, как UPEC, является неотъемлемым фактором развития ИМП.
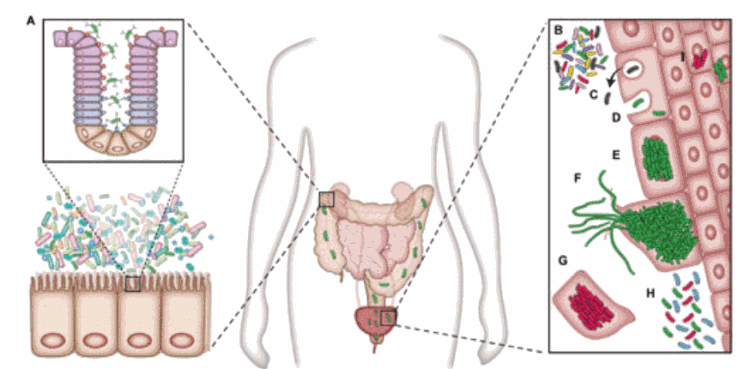
Во время инфицирования UPEC адгезируется и затем интернализуется в клетки уротелия (клетки, выстилающие стенку мочевого пузыря). В этом внутриклеточном убежище, защищенном от иммунных реакций хозяина, бактерии размножаются. В конце концов они выходят из клеток, чтобы соединиться с соседними клетками и заразить их. Чтобы справиться с этим непрошеным вторжением, эпителиальные клетки мочевого пузыря подвергаются запрограммированной клеточной гибели, и начинается эксфолиация (отшелушивание) эпителия. Эта борьба между бактериями и клетками мочевого пузыря приводит к появлению таких симптомов ИМП, как жгучая боль при мочеиспускании, кровь в моче и учащенное мочеиспускание.
В процессе отшелушивания инфицированные клетки удаляются, но при этом клетки эпителия подвергаются воздействию UPEC. Некоторые из этих бактерий проникают во вновь открытые клетки мочевого пузыря и образуют внутриклеточные резервуары покоя (quiescent intracellular reservoirs - IQR), в которых они живут до 12 недель. По мере обновления клеток мочевого пузыря бактерии в IQR могут вновь активизироваться и запустить новые инфекции.
Выживанию UPEC в мочевом пузыре способствуют также их физиологические и метаболические особенности. Бактерии оснащены пилями для прикрепления к клеткам хозяина, двухкомпонентными системами для восприятия и реагирования на окружающую среду, токсинами, системами выделения и способностью получать и использовать питательные вещества в моче (жидкости, лишенной многих соединений, которыми любят питаться другие бактерии). Хотя UPEC является основным возбудителем ИМП, другие бактерии, вызывающие ИМП, имеют свои собственные качества и причуды, которые способствуют выживанию и сохранению жизнеспособности. Например, P. mirabilis, частая причина катетер-ассоциированных ИМП, снабжена придатками, называемыми фимбриями, которые позволяют бактерии прилипать к поверхности эпителия и поверхности катетеров.
Избавление от ИМП - это не только комфорт, но и здоровье: патогенные микроорганизмы могут попасть из мочевого пузыря в почки и, возможно, в кровоток, создавая риск развития сепсиса. Задача состоит в том, чтобы взять ИМП под контроль до того, как она достигнет этой стадии.
Антибиотики в настоящее время являются основным средством лечения ИМП, но кризис резистентности к противомикробным препаратам снижает их надежность. Один из аспектов исследований направлен на разработку вакцин для профилактики ИМП. Некоторые перспективные кандидаты направлены на различные компоненты возбудителей ИМП. Например, клинические испытания фазы 1b показали, что у пациентов с ИМП вакцина SEQ-400, содержащая белок адгезина E.coli FimH, который необходим для адгезии и инвазии бактерий в клетки хозяина, способствовала снижению общего числа ИМП и ИМП, вызванных этой бактерией, на ~70%.
Другие вакцины содержат цельные термически инактивированные клетки распространенных возбудителей ИМП (например, E. coli, Enterococcus faecalis, Klebsiella pneumoniae и других). Один из таких кандидатов, MV140 (Uromune), представляет собой спрей со вкусом ананаса, который ежедневно принимается через рот. Испытание 3-й фазы показало, что среди женщин страдающих рецидивирующими ИМП, 58% не заболели ИМП после 6 месяцев применения MV140 по сравнению с 25% в группе плацебо.
В настоящее время также открываются и исследуются неантибиотические препараты для смягчения последствий рецидивирующих ИМП. К ним относятся молекулы, имитирующие белки на поверхности клеток хозяина, что позволяет связать микробы до того, как они инфицируют клетки, а также соединения, полученные из различных источников, например растений. В недавнем исследовании были обнаружены 2 соединения растительного происхождения, которые нарушают механизмы клетки-хозяина, необходимые для проникновения UPEC в клетки мочевого пузыря. Это самое главное: если бактерии не могут проникнуть в клетки, они не смогут защититься от антибиотиков. Авторы исследования предполагают, что растительные соединения можно назначать вместе с антибиотиками, чтобы усилить их действие.
Аналогичное обоснование лежит в основе интереса ученых к фаговой терапии - терапевтическому использованию вирусов, заражающих бактерии, для смягчения последствий ИМП. Часто бактерии развивают резистентность к заражающим их фагам, но при этом они становятся более чувствительными к антибиотикам. Использование этого компромисса может стать способом сохранить эффективность существующих методов терапии.
Все это говорит о том, что будущее, в котором не будет рутинных инфекций, не является чем-то несбыточным. Чем больше ученые будут узнавать о механизмах, лежащих в основе рецидивирующих инфекций, тем больше возможностей будет появляться для того, чтобы избавиться от них навсегда.