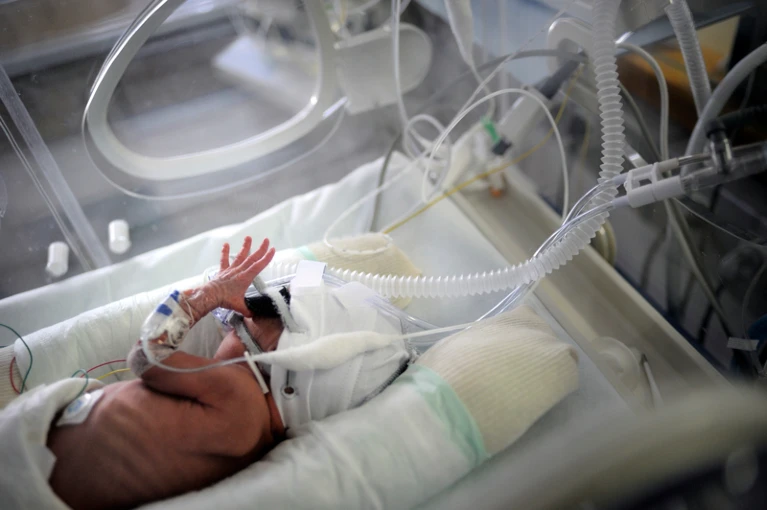
Оптимизированные рабочие процессы секвенирования ДНК и РНК помогают врачам оказывать оперативную и адресную помощь людям за считанные дни или даже часы.
Иногда хорошие новости приходят слишком поздно. Около десяти лет назад клинический генетик Зорница Старк и ее коллеги из Детского научно-исследовательского института Мердока в Мельбурне (Австралия) задались целью узнать, как секвенирование генома может улучшить лечение маленьких детей с подозрением на наследственные заболевания. Исследователи секвенировали белково-кодирующие области в геномах 80 младенцев в поисках генетических изменений, объясняющих их состояние. У одного девятимесячного мальчика с тяжелыми неврологическими симптомами группа Старк обнаружила мутацию, которая приводила к дефициту витамина B1, что можно было легко вылечить с помощью добавок за 150 австралийских долларов в год (136 долларов США в то время).
К сожалению, для получения ответа потребовалось шесть месяцев с момента взятия образца. Лечение витамином B1 позволило мальчику выжить, но за это время его состояние ухудшилось, и он остался инвалидом на всю жизнь. "Даже при двух-трехнедельном сроке выполнения заказа это все равно недостаточно быстро для лечения многих заболеваний", - говорит Старк. "Я очень хотела сделать это еще быстрее".
Сегодня этот метод действительно работает гораздо быстрее. Старк и другие специалисты по всему миру неоднократно демонстрировали целесообразность и клиническую пользу быстрого секвенирования и интерпретации для своевременного и персонализированного вмешательства в ранее неизученные заболевания. Как правило, такие рабочие процессы позволяют поставить диагноз менее чем за неделю, но рекорд по времени постановки диагноза на основе секвенирования генома, принадлежащий исследователю геномики Юэну Эшли из Стэнфордского университета в Калифорнии и его коллегам, составляет чуть более семи часов. А когда в онкологии требуется сверхбыстрая диагностика, рабочие процессы даже помогают врачам классифицировать опухоли и планировать лечение менее чем за час.
Некоторые врачи, особенно склонные к консервативному подходу, с трудом соглашаются на диагностику с помощью секвенирования. Еще десять лет назад анализ генома был медленным, дорогим и вряд ли давал практические результаты. Но скептики постепенно успокаиваются. "Когда я разговариваю с сотрудниками клиник, они всегда говорят: "А, нам это не нужно", - делится Йерун де Риддер, биоинформатик из Университетского медицинского центра Утрехта (Нидерланды), разработавший на основе секвенирования методику оказания помощи при опухолях мозга в течение 90 минут после взятия биоптата. "Но когда вы создаете условия для этого и делаете это возможным, они вдруг начинают видеть перспективы, которых раньше не замечали".
Технологии развиваются так быстро, что даже тем, кто только начинает их внедрять, бывает трудно угнаться за ними.
"Каждые 18 месяцев или около того происходит технологическая революция - не эволюция, а революция",
- отмечает Стивен Кингсмор, пионер в области быстрого секвенирования в Детском институте геномной медицины Рэди в Сан-Диего. "Сейчас развитие генных технологий находится в самом разгаре".
Генетические диагностические анализы служат руководством для клиницистов уже несколько десятилетий. Первые тесты были нацелены на гены с известной связью с заболеванием, такие как ген BRCA1, определяющий риск развития рака груди. Но по мере снижения стоимости секвенирования все более популярным становится тестирование всего генома для диагностики рака или редких генетических заболеваний. Однако колеса этого процесса вращаются медленно. "Ничто в клиническом генетическом тестировании не было создано с расчетом на скорость, - считает Эшли.
Секвенирование миллиардов нуклеотидов с достаточной "избыточностью", чтобы обеспечить высокую точность результатов, требует времени, а тщательное изучение результатов для выявления потенциально значимых аберраций последовательностей - еще больше времени. Даже более целенаправленный анализ "экзома", который фокусируется на 1-2% генома, содержащего гены, кодирующие белки, требует месяцев для получения ответов.
Свою первую попытку ускорить процесс Кингсмор называет "случайной". В 2012 году компания Illumina, занимающаяся секвенированием, обратилась в тогдашнее учреждение Кингсмора - Детскую больницу милосердия в Канзас-Сити, - чтобы протестировать новый "режим быстрого выполнения". Компания Illumina была и остается лидером на рынке секвенирования с коротким прочтением - процесса, в результате которого получаются миллиарды 100-200-нуклеотидных "прочтений" последовательностей ДНК, которые затем могут быть вычислительным путем собраны в целые геномы или экзомы. Этот способ сочетает в себе достижения в области аналитической химии и секвенирования, что позволяет упростить и сократить этапы секвенирования примерно с 10 дней до одного. Кингсмор и его коллеги построили диагностический процесс на основе нового метода, который позволил им выявлять вероятные мутации, вызывающие заболевания у тяжелобольных новорожденных детей, в течение 50 часов после взятия образца крови.
"В трех из первых четырех случаев, когда мы расшифровали геномы, были поставлены диагнозы, и это было как взрыв бомбы", - вспоминает Кингсмор. С тех пор он продолжает совершенствовать процесс, публикуя десятки исследований и координируя испытание под названием Baby Bear, которое продемонстрировало возможность внедрения этого диагностического процесса на примере почти 200 новорожденных в 5 калифорнийских больницах в период с 2018 по 2020 год. По его оценкам, в настоящее время эту услугу ежегодно получают тысячи детей в Соединенных Штатах.
Другие группы разработали аналогичные программы. Группа Старк координирует программу Acute Care Genomics для младенцев и детей во всех австралийских больницах, а клинический генетик Ахмад Абу Таюн из детской специализированной больницы Al Jalila в Дубае возглавляет программу Little Falcon, в рамках которой 200 ближневосточных семей с тяжелобольными детьми будут проходить экспресс-секвенирование. В Великобритании клинический генетик Эмма Бэпл из Эксетерского университета координирует программу Национальной службы здравоохранения, в рамках которой ежегодно будет проводиться экспресс-секвенирование для 1200 семей в Англии и других частях Соединенного Королевства.
Чтобы добиться ускорения рабочих процессов, команды клинических генетиков выявили множество возможностей для рационализации процесса. Например, они в основном отказались от секвенирования экзома, которое требует дополнительных этапов подготовки образца и жертвует ценной информацией. "С тех пор как мы перешли на секвенирование всего генома, мы ставим на 3-4% больше новых диагнозов, которые не были бы обнаружены при секвенировании экзома", - рассказывает Бэпл. Сюда входят важнейшие мутации, которые находятся вне кодирующих областей и влияют на экспрессию и регуляцию генов".
Инструменты для секвенирования также стали намного быстрее. Многие лаборатории используют новейший прибор NovaSeq X Plus компании Illumina, который способен выдавать триллионы нуклеотидов данных о последовательностях в день. Но это может быть дорого - экономические преимущества таких высокопроизводительных систем проявляются при одновременной обработке большого количества образцов. Но большинство образцов для экспресс-секвенирования представляют собой отдельные срочные случаи, и поэтому секвенирование стоит столько же, сколько и секвенирование десятков геномов в стандартном рабочем процессе.
Каким бы ни был рабочий процесс, эти программы быстрого секвенирования достигают удивительно стабильного успеха, обычно позволяя поставить точный диагноз в 40-50% случаев, многие из которых могут быть решены медикаментозно. Интерпретация может быть сложной, но и она становится проще благодаря миллионам клинически аннотированных геномов и экзомов, собранных в рамках таких инициатив, как программа UK Biobank и база данных Genome Aggregation Database.
Этому также способствует постоянно развивающийся набор вычислительных методов. Предварительная обработка и анализ генома теперь могут выполняться с помощью облачных ресурсов, что избавляет исследователей от необходимости использовать дорогостоящие высокопроизводительные компьютеры. Развиваются и программные пакеты, автоматизирующие важнейшие этапы анализа. Например, Кингсмор и Абу Таюн используют инструментарий DRAGEN компании Illumina для быстрого нахождения релевантных вариантов последовательностей и структур. Существуют также полезные ресурсы, такие как GeneMatcher, онлайн-сервис, который помогает генетикам и клиницистам по всему миру обмениваться информацией о мутациях, связанных с заболеваниями. Через несколько минут после того, как GeneMatcher помог поставить диагноз одному маленькому пациенту, группа Бэпл получила информацию о подобных мутациях у других детей с сердечным заболеванием, называемым дилатационной кардиомиопатией. "Запись о дилатационной кардиомиопатии означала, что этот ребенок потенциально может попасть в список на трансплантацию, когда он станет достаточно взрослым", - говорит она.
А еще есть перспективы искусственного интеллекта (ИИ). По оценкам Абу Таюна, генетики и другие специалисты тратят около часа на ручную проверку каждого генома, прежде чем поставить первый диагноз. Но возможности ИИ развиваются, и пройдет немного времени, прежде чем эта технология окажет серьезное влияние, прогнозирует Кингсмор. Системы искусственного интеллекта "кое-что упускают, допускают ошибки, но сейчас вы можете получить интерпретацию генома за 10-минут ", - говорит он. А пока "нам предстоит еще много работать с людьми".
Компания Illumina остается основой почти всех программ клинического секвенирования в мире, но у нее есть множество конкурентов. Хотя эти платформы еще слишком новы, чтобы иметь значимый клинический опыт, они могут открыть возможности быстрого секвенирования для пользователей, которые не могут позволить себе высокую стоимость анализа одного образца на NovaSeq X Plus, цена которого превышает 1 миллион долларов.
Кингсмор особенно рад прибору AVITI от компании Element Biosciences из Сан-Диего. Этот прибор рассчитан на среднюю пропускную способность и обеспечивает точность в расчете на одно основание, которая, по словам компании, соответствует или превосходит показатели Illumina. "Купив три прибора - а они стоят относительно недорого, около 250 000 долларов каждый, - вы получите 200 геномов", - говорит он. Для сравнения: всего десять лет назад секвенирование полного генома стоило около 10 000 долларов. "Это будет совершенно революционно".
Но, пожалуй, наибольший ажиотаж вызывают технологии "длинных прочтений", особенно те, что разработаны британской компанией Oxford Nanopore Technologies (ONT). Длинные прочтения ценны для документирования дупликаций, делеций и других структурных изменений генов, которые сложно зафиксировать с помощью методов коротких прочтений. Важно отметить, что эта технология также может быть использована для обнаружения других "омических" показателей, когда требуется сверхбыстрая реакция, например, при раке.
Вопрос нескольких минут
Сверхбыстрое секвенирование может стать основой для эффективного лечения рака. Хотя платформы, разработанные ONT, в основном предназначены для секвенирования ДНК, они могут извлекать и другие виды молекулярной информации, включая паттерны экспрессии генов и эпигенетические модификации хромосомной ДНК. Такие данные могут помочь врачам ускорить диагностику рака, позволяя принимать важнейшие решения о лечении не за несколько недель, а за несколько часов.
Например, детские опухоли мозга могут проявляться в нескольких формах, некоторые из которых более агрессивны и устойчивы к лечению, чем другие. "Вопрос для хирурга заключается в том, насколько агрессивно он будет действовать?" - объясняет Йерун де Риддер, биоинформатик из Университетского медицинского центра Утрехта (Нидерланды). "Буду ли я идти на все и рисковать, или я могу быть более консервативным?" Данные о последовательностях ДНК могут помочь классифицировать такие опухоли, но эпигеномные маркеры - особенно паттерны метилирования ДНК - гораздо более информативны, говорит Кингсмор.
Коллектив под руководством де Риддера разработал алгоритм глубинного обучения под названием Sturgeon, который исследователи обучили на миллионах смоделированных наборов данных, полученных из профилей метилирования ДНК пациентов. В прошлом году эта группа сообщила, что Sturgeon точно классифицировал 45 из 50 образцов опухолей всего за 40 минут секвенирования на приборе ONT MinION. Это достаточно быстро для того, чтобы врачи могли принимать решения о терапии, пока пациенты еще находятся под наркозом для биопсии, и при необходимости сразу приступать к агрессивной операции. Команда также протестировала этот подход в реальных интраоперационных условиях. По словам де Риддера, подобный подход может оказаться полезным и для других типов гетерогенных опухолей, включая саркомы мягких тканей.
Ученые также разрабатывают "жидкие биопсии" на основе секвенирования, при которых исследуются жидкости организма, такие как кровь и моча, для быстрого обнаружения, мониторинга и оценки реакции на лечение при раке. Группа под руководством вычислительного биолога Мартина Смита из Университета Нового Южного Уэльса (Австралия) показала, что секвенирование РНК с помощью MinION может сократить время профилирования образцов крови на лейкемию с нескольких дней до нескольких минут. "Для большинства образцов достаточно пяти минут, чтобы классификация превысила 90%, а это всего 30 000 прочтений", - говорит Смит. Алгоритм позволяет различать 11 подтипов острого лимфобластного лейкоза на обычном ноутбуке, и Смит говорит, что подобный подход может быть применен и к другим критическим по времени состояниям, включая сепсис, инфекции и аутоиммунные заболевания.
Приборы ONT генерируют данные о последовательности фрагментов ДНК, состоящих из тысяч оснований, отслеживая колебания электрического тока при прохождении ДНК через крошечные поры. Последовательности могут быть получены всего за несколько часов, и их можно даже анализировать по мере поступления данных в компьютер. "Это огромный скачок в плане времени секвенирования", - говорит Старк, которая надеется приступить к использованию ONT в следующем году. "Такие секвенаторы часто бывают портативными, так что было бы очень здорово перенести секвенирование ближе к постели больного". Речь идет о приборе ONT MinION, который по размеру примерно равен мобильному телефону.
Группа Эшли использовала высокопроизводительную настольную систему PromethION компании ONT для постановки рекордных геномных диагнозов. Выделив целый цикл секвенирования для одного образца, команда смогла сократить общее время секвенирования до нескольких часов. Однако оставалось несколько узких мест, и даже мощный компьютер с современным графическим процессором требовал 18 часов времени на анализ одного образца.
"Мы действительно рассматривали каждую часть процесса и спрашивали себя: есть ли способ сделать это быстрее?", - вспоминает Эшли. Это означало сокращение подготовки образцов практически до минимума и переход на облачную обработку данных для запуска таких алгоритмов, как DeepVariant - инструмент глубинного обучения, разработанный Google для быстрого выявления и классификации потенциальных генетических вариаций, связанных с заболеваниями. В лучшем случае время, необходимое для интерпретации последовательности, "может составлять всего десять минут", - говорит Эшли, хотя в более сложных случаях может потребоваться больше времени, если потребуется тщательная ручная оценка. В настоящее время его группа рассматривает возможность расширения и ускорения этого процесса, а несколько других групп начинают исследовательскую работу с ONT. "Я думаю, что нам удается получить 10-15% дополнительных диагностических результатов, в основном структурных и метилированных вариантов", - рассказал Абу Таюн об опыте своей группы.
Перезагрузка системы
Когда речь идет о клинической диагностике, технологии - это только половина успеха: необходимо также разобраться с человеческим фактором и логистикой.
"Самое узкое место - это заставить врачей понять, что это доступно и что это можно заказывать", - говорит Абу Таюн.
"И, конечно, убедиться, что, получив результаты, они смогут действовать в соответствии с ними". Это требует проработки множества других деталей, включая оптимальное соотношение между скоростью и стоимостью, а также того, действительно ли постановка диагноза менее чем за один день улучшает результаты по сравнению с тремя или пятью днями. Для тяжелобольных новорожденных с серьезными проблемами срочность очень важна, но есть соображения, выходящие за рамки самого исследования. "Конечно, хорошо ускорить проведение теста, чтобы он выполнялся менее чем за 10 часов, но если ребенку потребуется ждать 3 недели, чтобы сделать тест, вы не получите всех преимуществ", - говорит Старк.
Равный доступ также остается сложной проблемой. Перенос анализа данных в облако снимает вычислительное бремя с больниц. Но если на месте нет оборудования для секвенирования и квалифицированных пользователей, медицинским учреждениям с ограниченными ресурсами приходится отправлять образцы в централизованные лаборатории, что приводит к задержкам и логистическим препятствиям. По словам Эшли, это может дать преимущество доступным и портативным приборам ONT - особенно в сельских районах или странах с низким и средним уровнем дохода, где лабораторные ресурсы ограничены.
По мере развития рабочих процессов быстрого секвенирования эти проблемы должны разрешиться. А круг людей, которым это может быть полезно, огромен. В настоящее время Кингсмор применяет метод быстрого секвенирования генома для проверки десятков тысяч новорожденных на наличие почти 400 генетических заболеваний в рамках исследования, известного как BeginNGS. По его словам, этот проект отчасти является испытательным полигоном для новых технологий, призванных усовершенствовать этот процесс, включая инструменты, управляемые искусственным интеллектом, которые в настоящее время соответствуют примерно 90% диагностической точности экспертов-людей. Но в более широком смысле речь идет о том, чтобы проложить путь к будущему, в котором каждый сможет воспользоваться быстрым и точным секвенированием.
"Нам нужно что-то, что мы сможем делать на миллионах образцов в год менее чем за 1000 долларов, а может быть, и менее чем за 500 долларов", - говорит Кингсмор. "Мы должны думать об автоматизации в совершенно ином масштабе".