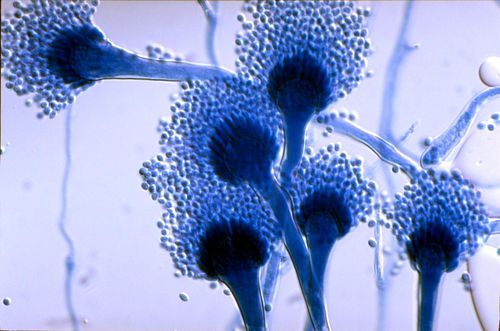
Ученые Массачусетского университета сделали важное генетическое открытие, которое проливает свет на применение препарата каспофунгин для лечения смертельно опасной грибковой инфекции Aspergillus fumigatus, от которой ежегодно умирают около 100 000 иммунокомпрометированных пациентов.
Как правило, здоровые люди вдыхают от 50 до 100 спор A. fumigatus каждый день, находясь на открытом воздухе. "Наш организм прекрасно справляется с их идентификацией и уничтожением", - говорит руководитель исследования Джон Гиббонс, чья лаборатория микробной геномики изучает этот грибок. Но у людей с ослабленной иммунной системой в результате лечения рака, трансплантации органов, ВИЧ, COVID-19 и других заболеваний A. fumigatus может вызвать "действительно неприятную инфекцию - инвазивный легочный аспергиллез, смертность от которого составляет 50%", - говорит Гиббонс. "А способы лечения этих инфекций ограничены".
Осложняет ситуацию то, что при введении в высоких концентрациях в качестве лечения инфекции A. fumigatus противогрибковый препарат иногда вызывает "парадоксальный эффект каспофунгина" [CPE], который усиливает рост грибка, а не уничтожает его. В исследовании, опубликованном в журнале Microbiology Spectrum, ученые описывают первый важный шаг в попытке понять, когда и почему терапия каспофунгином может принести больше вреда, чем пользы. Авторы впервые провели геномную и молекулярную идентификацию двух генов, которые способствуют парадоксальному эффекту у A. fumigatus.
"Это одно из первых исследований, в котором был применен полногеномный поиск ассоциаций (GWA) для идентификации генов, вовлеченных в фенотип Aspergillus fumigatus", - говорится в статье.
Исследователи секвенировали геном 67 клинических образцов, около половины из которых имели CPE, выявили генетические различия между группами, а затем с помощью статистического метода GWA определили, как эти генетические варианты связаны с особенностями роста при высоких концентрациях каспофунгина. "Мы определили несколько генов-кандидатов, которые, по нашему мнению, могут способствовать этому парадоксальному эффекту", - рассказывает Гиббонс.
Затем ученые использовали технологию генной инженерии CRISPR для удаления этих генов-кандидатов из генома, создав мутантов с делецией генов, что позволило исследователям определить, что два из этих генов участвуют в парадоксальном эффекте. "Похоже, что существует множество генов и множество генетических вариантов, которые способствуют развитию этого фенотипа", - говорит Гиббонс. "Мы еще не закончили. Одна из идей заключается в том, что мы можем потенциально создать новые мишени для препаратов, если найдем полный набор генов. Мы пока не понимаем механизмов полностью".
В конечном итоге команда надеется, что они смогут использовать секвенирование ДНК для понимания генетической основы различных фенотипов в целом и для предсказания клинических преимуществ, если образец пациента A. fumigatus имеет генотип, который связан с парадоксальным эффектом. "Это был бы важный инструмент, который мог бы действительно улучшить лечение", - утверждает Гиббонс.