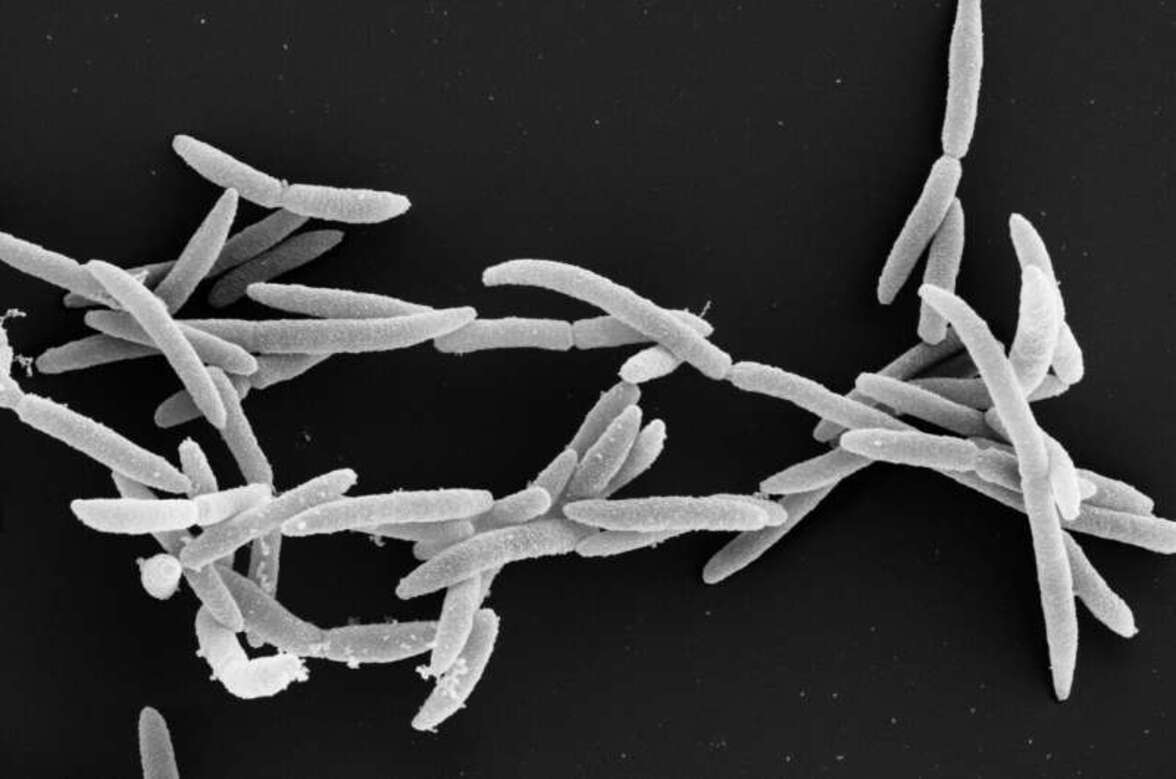
Фузобактерии являются комменсалами микробиома полости рта, которые могут распространяться из своей первичной ниши и колонизировать дистальные участки человеческого тела.
Их присутствие в тканях колоректального рака и рака молочной железы ассоциируется с ростом опухоли, метастазированием и устойчивостью к химиотерапевтическим препаратам. Использование неселективных антибиотиков для удаления фузобактерий препятствует прогрессированию опухоли, но длительное применение вызывает побочные эффекты, такие как желудочно-кишечные проблемы и дисбактериоз. Ученые из Института исследований инфекций имени Гельмгольца (Германия) работают над созданием инновационных стратегий, препятствующих распространению этих бактерий. В недавнем исследовании группа ученых под руководством Йорга Фогеля выявила соединение, которое эффективно останавливает рост пяти видов Fusobacterium. Результаты исследования были опубликованы в журнале mBio.
"Фузобактерии и в частности Fusobacterium nucleatum, долгое время оставались вне поля зрения, несмотря на их клиническое значение", - говорит Фогель. "Одной из целей нашей исследовательской группы является изучение стратегий, позволяющих целенаправленно уничтожать эти бактерии в карциномах". В своем недавнем исследовании ученые сосредоточили внимание на пептидной нуклеиновой кислоте, или ПНК. Это синтетические молекулы, похожие на ДНК или РНК. В отличие от природных нуклеиновых кислот, основа ПНК состоит из пептидной структуры, что придает ПНК исключительную стабильность. Основания остаются такими же, как в ДНК, что позволяет ПНК нацеливаться на транскрипты. Будучи антисмысловыми молекулами, ПНК связываются с комплементарной мессенджерной РНК (мРНК), блокируя ее функцию и подавляя выработку необходимых белков. Такое целенаправленное действие делает ПНК потенциально новым поколением антибактериальных агентов.
Исследованные антисмысловые молекулы, введенные для воздействия на конкретные гены, не смогли подавить рост бактерий. Однако исследовательская группа сделала неожиданное открытие: контрольное соединение FUS79, не нацеленное на конкретный транскрипт, проявляло сильную активность против пяти штаммов фузобактерий, не влияя на другие виды бактерий. «Результат оказался неожиданным, поскольку это соединение действует не так, как ожидается в случае цепочек антисмысловых нуклеиновых кислот, а имеет новый механизм», - объясняет Фогель. «Похоже, что оно оказывает свое действие, вызывая мембранный стресс, дестабилизируя мембрану бактериальной клетки или нарушая ее функцию, хотя нам еще предстоит изучить это более подробно».
Фогель добавляет, что «следующим нашим шагом будет расшифровка самого механизма действия этого соединения и его дальнейшая оптимизация для повышения эффективности». Исследование закладывает основу для разработки антисмысловой терапии против Fusobacterium nucleatum и подчеркивает потенциал этого соединения в качестве новой стратегии для более целенаправленного применения антибиотиков. Полученные данные могут ускорить дальнейшие исследования в этой области, что в конечном итоге улучшит результаты лечения рака.