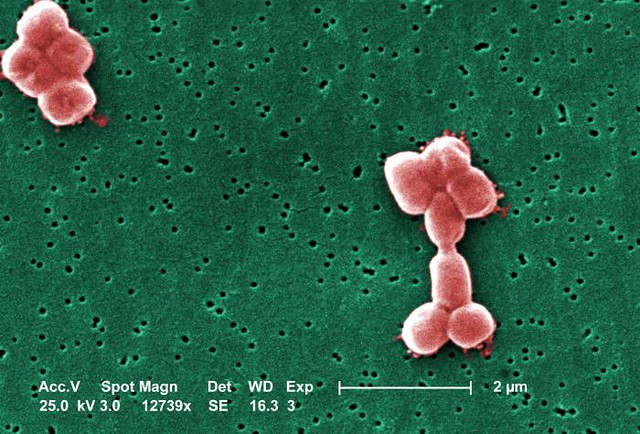
В течение многих лет эксперты в области общественного здравоохранения бьют тревогу по поводу следующего этапа сосуществования человечества с бактериями - мрачного будущего, в котором новые штаммы сделают некогда мощные антибиотики бесполезными.
Организация Объединенных Наций недавно спрогнозировала, что если не будут разработаны новые лекарства, то инфекции с множественной лекарственной устойчивостью заставят до 24 миллионов человек оказаться в крайней нищете в течение следующего десятилетия и станут причиной 10 миллионов ежегодных смертей к 2050 году.
Ученые особенно опасаются широкой группы бактерий, которые циркулируют в больницах и могут уклоняться не только от лекарств-блокбастеров, таких как пенициллин и тетрациклин, но даже от колистина, антибиотика, который долгое время использовался как последний вариант. Когда колистин не помогает, у пациентов с инфекциями с множественной лекарственной резистентностью часто не остается выбора эффективных антибиотиков.
Недавно ученые сообщили о своем открытии соединения, которое потенциально может преодолеть резистентность к колистину. В экспериментах на животных этот перспективный антибиотик обладал высокой эффективностью против опасных условно-патогенных микроорганизмов, таких как Acinetobacter baumannii, наиболее распространенной причины инфекций в медицинских учреждениях. Результаты исследования, опубликованные в журнале Nature, могут позволить разработать новый класс антибиотиков для борьбы со штаммами, не поддающимися никаким другим методам лечения.
Колистин давно и широко используется в животноводстве и в клинике. Считается, что его чрезмерное использование оказало сильное эволюционное давление на бактерии, в результате чего некоторые виды приобрели новый ген под названием mcr-1, который позволяет избежать токсичности колистина, и делает эти бактерии резистентными к препарату.
Устойчивость к колистину распространяется быстро, отчасти потому, что mcr-1 находится на плазмиде - кольце ДНК, которое не является частью основного бактериального генома и может легко передаваться от клетки к клетке. " Она переходит от одного штамма бактерий к другому или от инфекции одного пациента к инфекции другого", - говорит главный автор статьи Цзунцян Ванг.
Ванг и его коллеги задались вопросом, существуют ли природные соединения, которые можно использовать для борьбы с бактериями, резистентными к колистину. В природе бактерии постоянно соперничают за ресурсы, разрабатывая новые стратегии, чтобы противостоять конкурирующим штаммам. По сути, сам колистин вырабатывается почвенными бактериями для уничтожения конкурентов. Если соперник сопротивляется атаке, подхватывая mcr-1, нападающий микроорганизм может впоследствии приобрести новую мутацию, запустив новую версию колистина, способную убить бактерию с mcr-1.
"Мы отправились на поиски природных соединений, которые почвенные бактерии могли выработать для борьбы с собственной проблемой резистентности к колистину", - рассказывает Ванг. Его сотрудники использовали инновационный подход, который позволяет обойти ограничения традиционных методов поиска антибиотиков. Вместо того, чтобы выращивать бактерии в лаборатории и искать соединения, которые они производят, исследователи ищут в ДНК бактерий соответствующие гены.
Просмотрев более 10 000 бактериальных геномов, они обнаружили 35 групп генов, которые, по их прогнозам, могут производить соединения, похожие на колистин. Одна группа выглядела особенно интересной, поскольку включала гены, которые достаточно сильно отличались от тех, которые производят колистин, чтобы предположить, что они будут производить функционально отличную версию препарата. При дальнейшем анализе этих генов исследователи смогли предсказать структуру новой молекулы, которую они назвали маколацин. Затем они химически синтезировали этот неизвестный ранее родственник колистина, получив новое соединение без необходимости извлекать его из природного источника.
В лабораторных экспериментах было показано, что маколацин обладает мощным действием против нескольких типов бактерий, резистентных к колистину, включая Neisseria gonorrhoeae. Колистин, напротив, оказался абсолютно неэффективным в отношении этой бактерии. Затем ученые протестировали новый препарат на мышах, инфицированных резистентной к колистину XDR A. baumannii. Мыши, получившие инъекцию оптимизированного маколацина, полностью избавились от инфекции за 24 часа, в то время как мыши, получавшие колистин или плацебо, сохранили по крайней мере то же количество бактерий, что и при первоначальном заражении.
"Наши результаты показывают, что маколацин потенциально может быть разработан в качестве препарата для применения против некоторых из наиболее опасных патогенов с множественной лекарственной резистентностью", - говорит Ванг.
В другом исследовании этих же авторов использовались аналогичные методы для изучения другого класса антибиотиков, называемых менахинон-связывающими антибиотиками (MBA). В работе, опубликованной недавно в журнале Nature Microbiology, исследователи показали, что у мышей выявленные ими новые MBA эффективны против метициллин-резистентного Staphylococcus aureus, еще одной причины опасных инфекций в медицинских учреждениях.
Ванг добавляет, что метод эволюционного поиска генома, использованный для открытия маколацина, может быть применен и к другим проблемам лекарственной резистентности.
"В принципе, можно искать в бактериальной ДНК новые варианты любого известного антибиотика, который становится неэффективным из-за лекарственной резистентности штаммов."