Исследователи изучают, почему энергетические фабрики перемещаются между клетками и можно ли использовать этот процесс для лечения рака и других заболеваний.
В мире клеточной биологии наблюдается неожиданное оживление - в частности, в отношении энергетических фабрик, известных как митохондрии. С тех пор как они были открыты в середине XIX века, митохондрии считались органеллами, находящимися внутри клеток. Но теперь эта хрестоматийная картина представляется неверной. Бурный рост исследований ставит под сомнение давний образ митохондрий как исключительно клеточных органелл. «Они могут быть многоклеточными органеллами», - утверждает Джонатан Брестофф, иммунолог, изучающий метаболизм в Вашингтонском университете. Другими словами, эти якобы статичные энергетические фабрики теперь кажутся опытными путешественниками, переходящими из одной клетки в другую по первому требованию.
Этот «митохондриальный перенос» наблюдался в самых разных клетках и организмах, таких как дрожжи, моллюски и грызуны. "Это действительно захватывающее зрелище, - говорит Джеффри Спис, биолог стволовых клеток из Вермонтского университета. Пока неясно, почему митохондрии так мобильны. Некоторые исследования указывают на то, что клетки отдают свои митохондрии соседям в трудные времена. В чрезвычайных ситуациях митохондрии, прибывшие в клетку, могут запустить процесс восстановления тканей, стимулировать иммунную систему или спасти от гибели пострадавшие клетки. Другие исследования показывают, что перенос митохондрий может быть смертоносным оружием, которое раковые клетки используют, чтобы получить преимущество.
Но что это означает для здоровья человека, пока остается загадкой. Исследователи еще не выявили этот процесс внутри человеческого тела и поэтому не знают наверняка, происходит ли он у людей, замечает Дэниел Дэвис, иммунолог из Имперского колледжа Лондона. «У нас пока нет технологий, чтобы наблюдать за этим процессом», - говорит он. Этот факт не мешает исследователям изучать возможности использования переноса митохондрий для лечения различных заболеваний, включая рак и инсульт.
За последние три десятилетия исследования показали, что митохондрии - это не просто клеточные электростанции, которые превращают питательные вещества из пищи в энергию. Они являются ключевыми участниками множества процессов в организме: управляют процессом функционирования клеток и участвуют в иммунном ответе против вредоносных захватчиков. Они также неожиданно разнообразны. В прошлом году исследователи обнаружили, что митохондрии делятся на две разные формы, чтобы помочь клеткам выжить в условиях дефицита питательных веществ. Другое исследование, опубликованное в марте, смоделировало плотность и тип митохондрий в человеческом мозге.
Считается, что все митохондрии - в любом организме, в любой части тела - произошли от одной и той же древней бактерии. Около 1,5 миллиарда лет назад эта дрейфующая бактерия была поглощена микробом, который в итоге дал начало эукариотам - большой группе организмов, включая нас, клетки которых имеют изолированное ядро. После нескольких эволюционных поворотов эта заимствованная бактерия превратилась в органеллу, которая управляет метаболизмом. Микробное происхождение митохондрий, вероятно, помогает объяснить, почему они более динамичны, чем кажется на первый взгляд, поясняет Казухиде Хаякава, нейробиолог из Массачусетской больницы общего профиля, который изучает, как перенос митохондрий может помочь в лечении инсульта. «Возможно, митохондрии сохранили древнюю способность распространяться от клетки к клетке, подобно бактериям», - говорит он.
В 2006 году Спис и его коллеги впервые увидели, как митохондрии переходят из одной клетки в другую. Ученые пытались понять озадачивающее поведение стволовых клеток в лабораторных экспериментах. Казалось, что эти клетки обмениваются некой физической информацией, которая подсказывает им, как дифференцироваться, и предполагалось, что в этом участвуют митохондрии. Чтобы выяснить роль митохондрий, исследователи культивировали клетки рака легких человека, в которых отсутствовали эти органеллы, вместе со стволовыми клетками, полученными из костного мозга. Пометив митохондрии стволовых клеток флуоресцентными белками, исследователи сняли таймлапс-видео, чтобы увидеть, что происходит дальше. На зернистых черно-белых кадрах было видно, как стволовые клетки выбрасывают свои митохондрии, которые затем поглощаются дефектными клетками легких. После такого донорства клетки легких быстро восстановили свою способность делиться и превращать глюкозу в энергию. «Наблюдение за этим было похоже на чудо», - вспоминает Спис.
С тех пор исследователи наблюдали, как митохондрии молниеносно перемещаются между несколькими типами клеток - легочными, сердечными, мозговыми, жировыми, костными и другими. Иногда митохондрии путешествуют по эфемерным магистралям, известным как туннельные нанотрубки, которые образуются между клетками и переносят другие клеточные грузы. В других случаях митохондрии путешествуют в пузырьках-везикулах или свободно плавают в крови. Как митохондрии выходят из строя, в основном выяснено, но менее понятно, почему. По словам Клэр Кру, клеточного биолога из Вашингтонского университета, исследователи выясняют, что этот процесс часто является формой контроля клеточных повреждений.
Некоторые исследования показывают, например, что перенос митохондрий может помочь клеткам пережить неврологические бури. В 2016 году Хаякава и его коллеги обнаружили, что у мышей, перенесших инсульт, опорные клетки, называемые астроцитами, доставляют свои митохондрии к слабеющим нейронам. Благодаря этой митохондриальной подпитке нейроны отращивали отростки и перезапускали обменные процессы, что повышало их шансы на выживание. Когда исследователи подавляли передачу митохондрий, выживало меньше нейронов, что говорит о том, что пожертвованные органеллы были ключом к восстановлению клеток. Но какая часть структуры или функции митохондрий защищала клетки, пока неизвестно.
По утверждению Джахара Бхаттачарии из Колумбийского университета в Нью-Йорке, специализирующегося на тяжелых воспалительных заболеваниях, известных как острое повреждение легких, митохондриальная подпитка может быть полезна и клеткам легких во время кризиса. Он и его коллеги обнаружили, что у мышей с таким воспалением стромальные клетки, из которых состоят соединительные ткани, поддерживающие органы, передают свои митохондрии клеткам легких. Клетки с одолженными органеллами имели более высокую концентрацию клеточного топлива АТФ, которое в итоге распределялось между соседними клетками, не получившими новых митохондрий. Эти больные легкие показали больше признаков восстановления, чем больные легкие, не получившие митохондрии извне. Бхаттачария был поражен, когда он и его сотрудники наблюдали перенос митохондрий в действии. «Не думаю, что мы спали следующие несколько ночей, настолько это было захватывающе», - вспоминает он.
Другие исследования указывают на то, что перенесенные митохондрии могут ускорить заживление ран. В 2021 году Анн-Мари Родригес, клеточный биолог из Университета Сорбонны в Париже, и ее коллеги обнаружили, что тромбоциты, выделенные из человеческой крови, передают свои митохондрии стволовым клеткам, когда исследователи помещают эти два типа клеток вместе. Приняв митохондрии, стволовые клетки высвобождают молекулы, которые играют роль в формировании новых кровеносных сосудов. Когда клетки поместили на раны на коже мышей, они зажили быстрее, чем у грызунов, которым вводили либо стволовые клетки, либо только тромбоциты. Исследователи предполагают, что клетки с дисфункциональными митохондриями могут даже иметь возможность запрашивать здоровые митохондрии у своих соседей, хотя точные механизмы, лежащие в основе этого процесса, остаются туманными. "Мы только начинаем понимать, какие сигналы при этом задействованы, - говорит Родригес.
Помимо роли в восстановлении организма, исследователи хотят узнать, является ли перенос митохондрий важной частью повседневной биологии. Первые данные свидетельствуют о том, что он может способствовать поддержанию здоровья тканей. В прошлом году Минхао Чжэн, биолог-регенератолог из Университета Западной Австралии, и его коллеги обнаружили, что некоторые типы астроцитов отдают свои митохондрии клеткам, выстилающим кровеносные сосуды в мозге мышей. Когда исследователи нарушили этот процесс, гематоэнцефалический барьер стал негерметичным, что говорит о том, что передача митохондрий помогает поддерживать этот защитный мембранный экран. Чжэн и его коллеги уже сообщали, что перенос митохондрий в кости мышей может ускорить формирование новых кровеносных сосудов.
Брестофф и его сотрудники сообщили, что у здоровых мышей белые жировые клетки передают свои митохондрии макрофагам, которые собирают клеточный мусор. У мышей с ожирением количество перемещаемых органелл уменьшилось. Кроме того, мыши с ожирением сжигали меньше энергии, чем их здоровые сородичи. По мнению Брестоффа, эти органеллы могут помогать макрофагам функционировать, когда их метаболизм нарушен.
В лабиринтах иммунной системы донорские митохондрии могут оказывать противовоспалительное действие, особенно когда их поглощают Т-клетки, которые борются с инфекциями. В ходе исследований на клеточных культурах Патрисия Алехандра Луз-Кроуфорд, иммунолог из Университета Анд (Чили), и ее коллеги обнаружили, что некоторые типы Т-клеток, получившие митохондрии от стволовых клеток, вырабатывают меньше воспалительных молекул. Стволовые клетки, культивированные у людей с ревматоидным артритом, передают Т-клеткам меньше митохондрий, чем стволовые клетки здоровых людей, что, по ее словам, может способствовать хроническому воспалению, связанному с этим заболеванием.
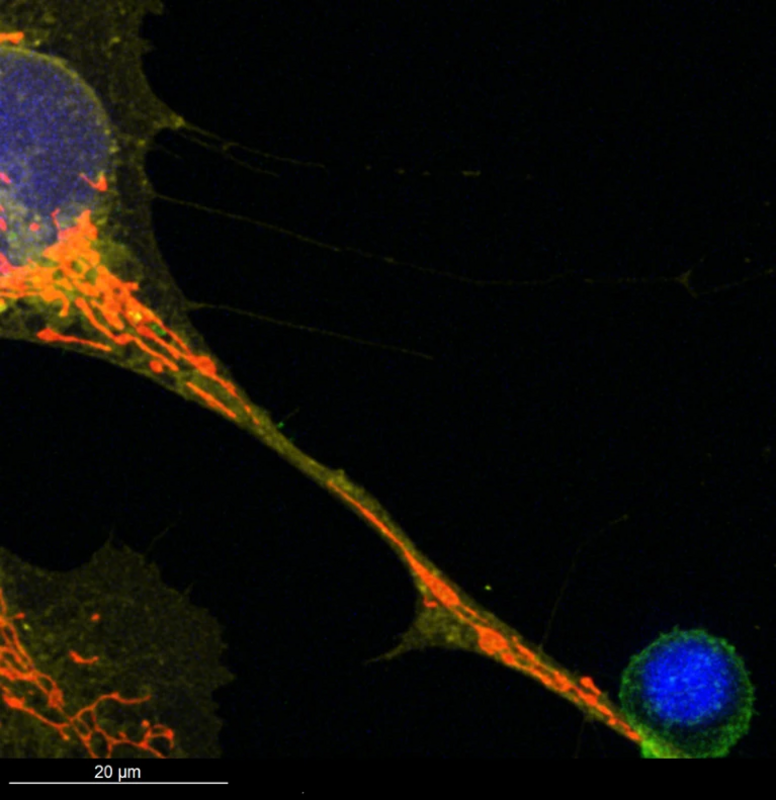
Митохондрии, выделенные красным цветом, перемещаются по туннельной нанотрубке от типа клеток костного мозга (вверху слева) к Т-клеткам, которые борются с инфекциями и раком (внизу справа). Фото: Jeremy Baldwin
Но в отношении переноса митохондрий остается много вопросов без ответа, в том числе вопрос о том, что могут делать органеллы после того, как они попадают в клетки, и как долго они существуют, говорит Луз-Кроуфорд. «Здесь все еще много загадок». Отсутствие подробной информации о том, почему клетки переносят свои митохондрии, не позволяет понять, какую конкретную роль эти клеточные обмены могут играть в таких заболеваниях, как сердечно-сосудистые заболевания и ожирение. В исследованиях in vivo митохондрии отслеживались лишь в нескольких типах тканей, что затрудняет построение общей картины того, какое влияние эти переносы оказывают на здоровье. Большинство существующих исследований рассматривают корреляции: они фиксируют, как клетки отличаются от других после получения донорских органелл. Но они не позволяют доказать, что переданные митохондрии вызывают клеточные изменения, считает Хосе Антонио Энрикес Домингес, молекулярный биолог из испанского Национального центра сердечно-сосудистых исследований.
У исследователей есть и другие вопросы по поводу трансфера. Хотя это может показаться благотворительным актом, исследования показывают, что некоторые клетки выбрасывают митохондрии как отходы. В других случаях клетки могут захватывать митохондрии извне, чтобы получить преимущество. Что именно заставляет клетки выбрасывать свои митохондрии, а что позволяет другим принимать их, пока неизвестно, добавляет Энрикес Домингес. По его мнению, необходимо также изучить возможные негативные последствия. В ряде исследований было высказано предположение, что раковые клетки могут похищать митохондрии у других клеток организма. В этой более злонамеренной модификации перенос митохондрий, по-видимому, помогает раковым клеткам избегать иммунной системы и становиться более инвазивными и устойчивыми к лечению. Исследования также показали, что раковые клетки быстрее размножаются после захвата митохондрий из других клеток.
Хотя за пределами клеточных культур этот факт пока не подтвержден, есть первые данные о том, что перенос митохондрий может происходить и у людей. Десять лет назад исследователи обнаружили митохондрии, свободно плавающие в человеческой крови. А в январе исследование, в ходе которого были взяты пробы митохондрий у небольшой группы людей с раком, показало, что у некоторых участников иммунные клетки, атакующие опухоль, содержали генетически мутировавшие митохондрии раковых клеток, что, по-видимому, препятствовало способности иммунных клеток бороться с заболеванием.
Препятствия на пути обнаружения и понимания митохондриального переноса, по крайней мере, частично связаны с технологическими ограничениями. Флуоресцентные белковые метки, которые могут подсвечивать митохондрии, считаются золотым стандартом, но поскольку они могут изменять функцию митохондрий, их слишком рискованно использовать на людях. Анализ последовательностей митохондриальной ДНК (мтДНК) из клеток-доноров и клеток-акцепторов - единственный надежный метод, позволяющий сделать вывод о переносе митохондрий внутри человеческого организма. Но перемещение генетического материала не означает, что перемещение совершила вся органелла, поясняет Брестофф.
Несмотря на неизвестность, многие исследователи, изучающие митохондриальный перенос, уверены, что он хотя бы иногда происходит у людей. Их исследования базовой биологии этого процесса во многом продиктованы желанием использовать его для улучшения здоровья человека. Если окажется, что перенос митохондрий является одним из основных биологических процессов в организме, это может открыть несколько потенциальных путей лечения, полагает Джереми Болдуин, иммунолог из Института иммунотерапии Лейбница (Германия). «Возможности безграничны».
В течение многих лет исследователи проверяли идею пересадки здоровых митохондрий непосредственно в клетки для лечения заболеваний, связанных с дисфункцией митохондрий. К ним относятся редкие генетические заболевания, такие как синдром Лея, при котором гибель нервных клеток вызывает судороги и задержку развития, а также болезни сердца и инсульты. Другие исследователи опробовали подход под названием «митохондриальная аугментация», при котором здоровые митохондрии помещаются в больные стволовые клетки человека в лабораторных условиях, а затем стволовые клетки вводятся обратно в организм человека.
Несколько исследователей приступили к разработке методов лечения, которые будут опираться на собственные возможности организма по переносу митохондрий. Например, однажды этот процесс можно будет использовать для усиления существующей Т-клеточной терапии, которая использует собственные иммунные клетки человека для борьбы с раком. В прошлом году Болдуин и его коллеги культивировали стромальные клетки совместно с Т-клетками. Стромальные клетки передали свои митохондрии Т-клеткам через нанотрубки, что повысило метаболическую активность Т-клеток. Эти заряженные Т-клетки разрушали опухоли у мышей более эффективно, чем те, которые не получали митохондрий, и демонстрировали меньше признаков истощения.
Другие исследователи стремятся убедить клетки пожертвовать свои митохондрии. В прошлом году Брестофф и его коллеги пересадили костный мозг здоровых мышей мышам с синдромом Лея. Трансплантация заставила стволовые клетки крови высвободить свои митохондрии, которые, покинув костный мозг, попали в клетки нескольких органов. Пересадка митохондрий была связана с улучшением неврологических функций и повышением выживаемости мышей. Пока неясно, как удалось добиться такого переноса, но результаты исследования позволяют предположить, что это вполне осуществимый метод лечения. Однако прежде чем подобные методы лечения появятся в клинике, исследователям необходимо лучше понять суть переноса митохондрий. Они должны будут точно определить конкретные механизмы. И им нужно будет разработать методы отслеживания терапевтических митохондрий по мере их перемещения от клетки к клетке, а возможно, и в другие органы и ткани.
«Вероятно, работа над расшифровкой всей этой биологии займет десятилетия», - отмечает Брестофф.

