Заживление ран - это многостороннее биологическое явление, позволяющее организму восстанавливать поврежденные ткани.
Клетки (кератиноциты, фибробласты и макрофаги) направляются к месту раны в результате воспалительной реакции и запускают процесс заживления через взаимодействие со стволовыми клетками. Это приводит к различным биохимическим процессам, которые позволяют организму регенерировать ткани. Чаще всего раны инфицируются Staphylococcus aureus, который может развивать резистентность к метициллину и антибиотикам (лактамам) благодаря проявлению чужеродного пенициллин-связывающего белка (PBP, PBP2a).
MRSA является серьезной проблемой здравоохранения во всем мире, а инфекции, вызванные этими микроорганизмами, относятся к числу наиболее сложных терапевтических задач. Инфекции, вызванные бактериальными биопленками, становятся все более распространенными во всем мире. Бактерии в биопленках часто устойчивы к стандартной антибиотикотерапии, поскольку со временем они выработали ряд защитных механизмов против обычной антибиотикотерапии. Развитие биопленок и антибиотикорезистентности имеет решающее значение для успеха борьбы с S. aureus.
Метициллин-резистентный Staphylococcus aureus (HA-MRSA и CA-MRSA) - это больничные и внебольничные инфекции, которые могут поражать различные части тела и варьировать по степени тяжести от незначительных контаминаций кожи до смертельных инфекций, таких как бактериемия, инфекции кожи и мягких тканей, инфекции костей и суставов, эндокардит, пневмония и сепсис. Ежегодно регистрируется около 20-50 случаев бактериемии S. aureus на 100 000 населения, что само по себе является причиной большего числа заболеваний, чем СПИД, туберкулез и вирусный гепатит вместе взятые.
В последние годы MRSA выделяется в основном из раневых культур и может резко замедлить заживление ран и повысить риск осложнений. Во-первых, воспаление, вызванное бактериями, может повреждать здоровые ткани и препятствовать процессу заживления. Во-вторых, MRSA может образовывать на ране биопленку, которая защищает микроорганизмы от иммунного ответа организма и затрудняет доступ антибиотиков к бактериям и их уничтожение. Лечение ран, инфицированных MRSA, обычно включает в себя сочетание антибиотиков и ухода за раной. Для лечения инфекции может быть назначен ванкомицин и другие антибиотики.
Для эффективного лечения ран и инфекций были разработаны и внедрены различные биологические стратегии. Среди них - использование различных скаффолдов, носителей и пластырей, изготовленных из водорослей, а также стимулирующих чувствительных гидрогелей и модифицированных церием (CeO2) наночастиц. Лишь небольшое количество антибиопленочных стратегий используется в клинических условиях, а остальные еще нуждаются в значительном развитии. Xiu et al. (2021) предложили использовать нанотехнологии для борьбы с бактериальными биопленками.
Пробиотики улучшают состояние здоровья при пероральном или местном применении и могут способствовать снижению риска заражения MRSA и улучшению исходов у пациентов с MRSA-инфекцией. Широкий спектр лактобацилл и бифидобактерий препятствует росту S. aureus и клинических изолятов MRSA in vitro. Однако для полной оценки потенциальных преимуществ пробиотиков в профилактике или лечении MRSA-инфекций необходимо провести дополнительные исследования.
Пробиотики, скорее всего, будут неэффективны у новорожденных и/или у людей с определенными клиническими проблемами, такими как рак, сахарный диабет, синдром негерметичного кишечника и выздоровление после трансплантации органов. Пробиотические штаммы могут обладать антибактериальной активностью в отношении MRSA. В одном из исследований было обнаружено, что пробиотический штамм Lactobacillus reuteri подавляет рост MRSA in vitro, а Lactobacillus plantarum предотвращает распространение MRSA у мышей.
Биоактивные молекулы, присутствующие в бесклеточном супернатанте молочнокислых бактерий, оказывают антистафилококковое действие, повышая уровень β-дефенсина и модулируя цитокины и хемокины на стадии заживления ран. Гидрогели, нагруженные Lactobacillus rhamnosus, значительно уменьшили инфекцию и воспаление, стимулировали производство нового коллагена и эпителия, а также ускорили заживление ран. Мыши, получавшие твердые липидные наночастицы, нагруженные куркумином, вместе с пробиотической повязкой (L. plantarum UBLP-40), демонстрировали более быстрое закрытие ран и меньшее количество биоповреждений в области раны. Благодаря иммуномодуляции, антибактериальной активности, подавлению патогенных токсинов и противовоспалительным свойствам эти препараты также способствуют заживлению ран.
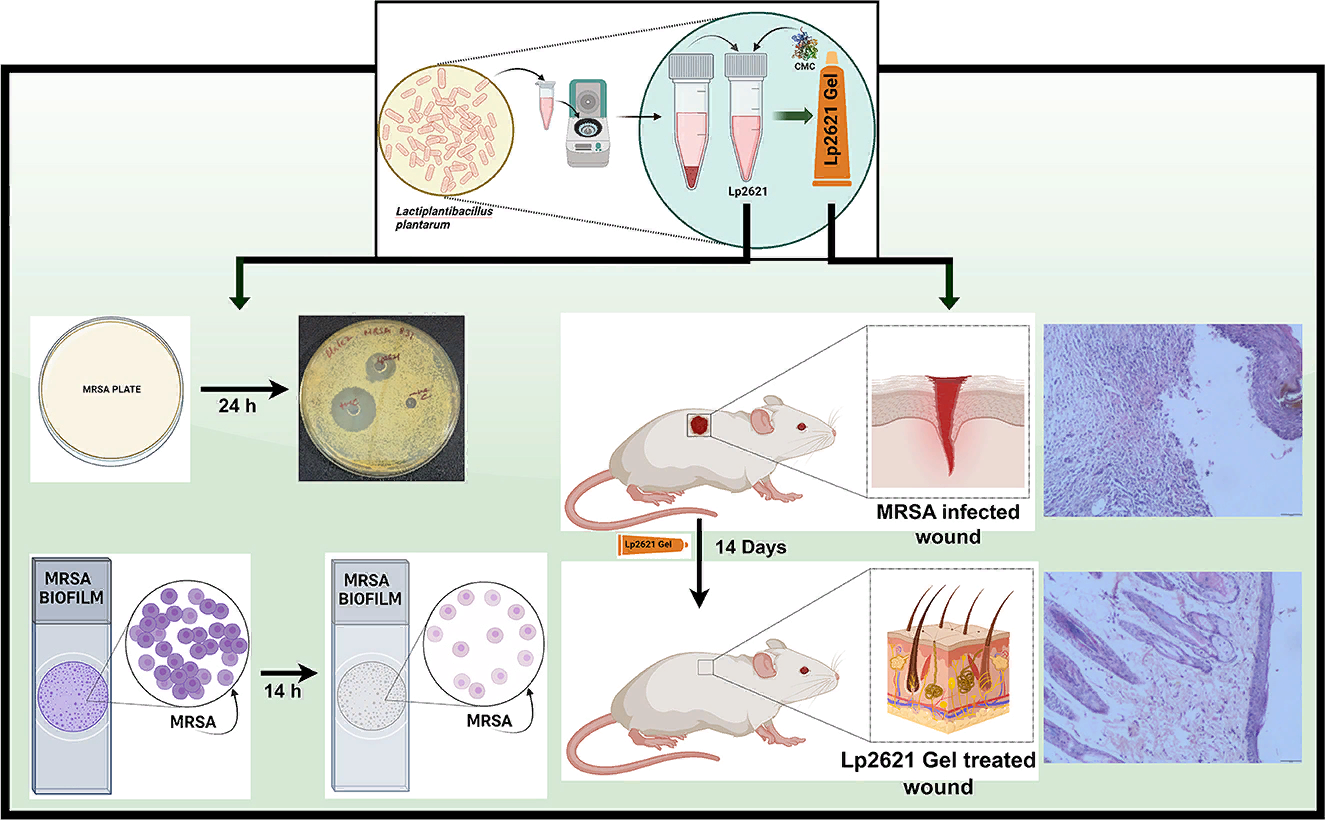
Ранее Lactiplantibacillus plantarum MTCC 2621 из нашей лаборатории продемонстрировал антимикробную активность, антиоксидантные свойства и ранозаживляющий потенциал бесклеточного супернатанта. В данном исследовании мы стремились оценить активность Lp2621 против MRSA, а также активность по уничтожению радикалов, ингибированию биопленки и эрадикации. Мы также представили доказательства того, что Lp2621 на мышиной модели способен заживлять эксцизионные раны, инфицированные MRSA.
Методы:
В настоящем исследовании мы оценили анти-MRSA, эффективность ингибирования и уничтожения биопленок, иммуномодулирующую активность в клеточной культуре THP-1 и ранозаживляющий потенциал в ранах, зараженных MRSA-инфекцией у мышей.
Результаты:
В анализе диффузии в агаровых лунках Lp2621 проявил анти-MRSA активность и показал дозозависимое ингибирование и уничтожение биопленки, что подтвердилось с помощью анализа с помощью конфокальной сканирующей лазерной микроскопии. Кроме того, Lp2621 в различных концентрациях проявлял иммуномодулирующую активность по экспрессии генов IL-6 и IL-10 в клетках THP-1. Аналогичные результаты были получены в образцах сыворотки крови мышей после обработки гелем Lp2621 иссеченной раны, инфицированной MRSA, что подтверждалось экспрессией цитокинов IL-6 (провоспалительный) и IL-10 (противовоспалительный).
Выводы:
В целом наши результаты показывают, что Lp2621 обладает мощными анти-MRSA и антиоксидантными свойствами и может предотвращать и устранять образование биопленок. Он также продемонстрировал хорошие результаты при применении на мышах с ранами, инфицированными MRSA.